题目内容
若某电能与化学能的转化装置(电解池或原电池)中发生的总反应的离子方程式是Cu+2H+═Cu2++H2↑,则下列关于该装置的有关说法中正确的是( )
| A、该装置可能是原电池,可用Cu、C作电极,电解质溶液是盐酸 |
| B、该装置可能是原电池,电解质溶液为硝酸 |
| C、该装置只能是电解池,金属铜为该电解池的阳极,K2SO4为电解质溶液 |
| D、该装置只能是电解池,金属铜为该电解池的阳极,稀H2SO4为电解质溶液 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:铜和弱氧化性酸不能自发的进行氧化还原反应,根据电池反应式知,铜和弱氧化性酸反应,则该装置是电解池,Cu作阳极,另一个电极是阴极,阴极上氢离子放电,则溶液中的阳离子是氢之前的金属阳离子或氢离子,据此分析解答.
解答:
解:铜和弱氧化性酸不能自发的进行氧化还原反应,根据电池反应式知,铜和弱氧化性酸反应,则该装置是电解池,Cu作阳极,另一个电极是阴极,阴极上氢离子放电,则溶液中的阳离子是氢之前的金属阳离子或氢离子,
A.该装置是电解池,故A错误;
B.该装置是电解池,且铜和稀硝酸反应生成NO而不是氢气,故B错误;
C.硫酸钾纯净物,属于电解质,不是电解质溶液,故C错误;
D.该装置是电解池,铜作阳极,硫酸是电解质,稀硫酸是电解质溶液,符合题意,故D正确;
故选D.
A.该装置是电解池,故A错误;
B.该装置是电解池,且铜和稀硝酸反应生成NO而不是氢气,故B错误;
C.硫酸钾纯净物,属于电解质,不是电解质溶液,故C错误;
D.该装置是电解池,铜作阳极,硫酸是电解质,稀硫酸是电解质溶液,符合题意,故D正确;
故选D.
点评:本题考查了原电池和电解池原理,明确原电池和电解池区别是解本题关键,不能自发进行的氧化还原反应可以设计成电解池来实现,易错选项是B,铜和稀硝酸反应不生成氢气,为易错点.

练习册系列答案
相关题目
下列离子方程式中正确的是( )
| A、盐酸与碳酸钡反应:CO32-+2H+=CO2↑+H2O |
| B、碳酸钙溶于醋酸:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、硝酸银溶液中加入铜粉:Ag++Cu=Cu2++Ag |
| D、钠投入水中:2Na+2H2O=2Na++2OH-+H2↑ |
某化学兴趣小组设计以下实验方案,可从样品中提取粗产品:
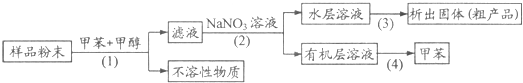
下列说法错误的是( )

下列说法错误的是( )
| A、步骤(1)需要过滤装置 |
| B、步骤(2)需要用到分液漏斗 |
| C、步骤(3)需要用到坩埚 |
| D、步骤(4)需要蒸馏装置 |
实验中安全意识是重要的科学素养,下列实验操作或事故的处理操作正确的是( )
| A、可以用饱和溴水除去苯中混有的苯酚 |
| B、不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| C、中和滴定时,应用待测液润洗滴定管和锥形瓶 |
| D、做完铜和浓硫酸反应的大试管实验结束时要立即往试管中加水清洗,这样可以减少尾气的产生 |
下列与实验相关的叙述正确的是( )
| A、用苯萃取溴水中的Br2时,有机层从分液漏斗的下端放出 |
| B、检验溶液中是否含有SO42-,依次滴入Ba(NO3)2溶液和稀盐酸 |
| C、配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
| D、配制AlCl3溶液时,将AlCl3溶解在较浓的盐酸中,再用水稀释到所需浓度 |
下列离子方程式中正确的是( )
| A、碳酸氢铵溶液与足量苛性钾溶液混合共热:NH4++OH-=NH3↑+H2O |
| B、Fe3O4溶解在过量的稀硝酸中:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| C、往硫酸铜溶液中加入过量的NaHS溶液:Cu2++2HS-=CuS↓+H2S↑ |
| D、石灰石溶解在醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
以烃和水为原料可以制得CO和H2,如CH4+H2O?CO+3H2.则下列关于甲烷与水反应的说法,正确的是( )
| A、CH4既被氧化又被还原 |
| B、H2O既不是氧化剂又不是还原剂 |
| C、在反应条件下,每消耗1mol H2O必然生成67.2L H2 |
| D、建立平衡后,使用更高效的催化剂,可使H2的产率提高 |
 为证明有关物质的性质,某学生设计了如图所示的装置.当打开活塞C,使液体A与隔板H上的固体B相遇时,即有气体产生,并发现D中蜡烛熄灭;关闭C 打开E时,则看到G中蜡烛燃得更亮,且F中盛放固体为淡黄色.
为证明有关物质的性质,某学生设计了如图所示的装置.当打开活塞C,使液体A与隔板H上的固体B相遇时,即有气体产生,并发现D中蜡烛熄灭;关闭C 打开E时,则看到G中蜡烛燃得更亮,且F中盛放固体为淡黄色.