题目内容
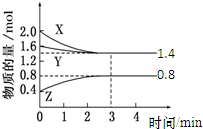 t℃时,在容积为2L密闭中充入X(g)、Y(g)与Z(g),反应过程中X、Y、Z的物质的量变化如下图所示.下列说法不正确的是( )
t℃时,在容积为2L密闭中充入X(g)、Y(g)与Z(g),反应过程中X、Y、Z的物质的量变化如下图所示.下列说法不正确的是( )| A、0~3 min,X的平均反应速率v(X)=0.2 mol?L-1?min-1 |
| B、发生反应的方程式可表示为:3X(g)+Y(g)?2Z(g) |
| C、保持其他条件不变,增大压强,平衡向正反应方向移动 |
| D、温度不变,增大X的浓度,该反应的平衡常数不变 |
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:A.根据容器体积,计算X的反应速率;
B.根据物质浓度变化的比例得到反应的化学方程式;
C.根据反应前后气体体积变化判断;
D.只有温度影响化学平衡常数.
B.根据物质浓度变化的比例得到反应的化学方程式;
C.根据反应前后气体体积变化判断;
D.只有温度影响化学平衡常数.
解答:
解:A、容器体积为2L,0~3 min,X物质的量变化为0.6mol,X的平均反应速率v(X)=
=0.1 mol?L-1?min-1,故A错误;
B、X、Y的物质的量均减小为反应物,变化量分别为:2.0-1.4=0.6mol,1.6-1.4=0.2mol,Z物质的量增大为生成物,变化量为:0.8-0.4=0.4mol,即三者的计量数之比为:3:1:2,化学方程式可写为:3X(g)+Y(g)?2Z(g),故B正确;
C、反应中反应物气体体积大于生成物气体体积,增大压强,平衡向正反应方向移动,故C正确;
D、化学平衡常数只与温度有关系,浓度变化不影响化学平衡常数,故D正确;
故选A.
| 0.6 |
| 2×3 |
B、X、Y的物质的量均减小为反应物,变化量分别为:2.0-1.4=0.6mol,1.6-1.4=0.2mol,Z物质的量增大为生成物,变化量为:0.8-0.4=0.4mol,即三者的计量数之比为:3:1:2,化学方程式可写为:3X(g)+Y(g)?2Z(g),故B正确;
C、反应中反应物气体体积大于生成物气体体积,增大压强,平衡向正反应方向移动,故C正确;
D、化学平衡常数只与温度有关系,浓度变化不影响化学平衡常数,故D正确;
故选A.
点评:本题考查化学平衡图象、化学方程式书写、平衡常数影响因素、化学反应速率的计算等,难度不大,注意掌握平衡移动原理.

练习册系列答案
相关题目
室温时,0.1mol?L-1的HA溶液的pH=3,向该溶液中逐滴加入NaOH,在滴加过程中,有关叙述正确的是( )
| A、原HA溶液中,c(H+)=c(OH-)+c(A-) |
| B、当滴入少量的NaOH,促进了HA的电离,溶液的pH降低 |
| C、当恰好完全中和时,溶液中c(Na+)>c(A-)>c(OH-)>c(H+) |
| D、当NaOH溶液过量时,可能出现:c(A-)>c(Na+)>c(OH-)>c(H+) |
下列各组物质,前者是混合物,后者是纯净物的是( )
| A、胆矾 玻璃 |
| B、汽油 液氯 |
| C、石油 盐酸 |
| D、干冰 铝热剂 |
下列各组物质中,前者属于电解质,后者属于非电解质的是( )
| A、NaCl溶液、CO2 |
| B、铜、蔗糖 |
| C、液态HCl、NH3 |
| D、汽油、硫酸溶液 |
下列有关叙述错误的是( )
A、水分子的结构式为 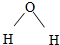 |
| B、氧与氟形成的化合物(OF2)中,氧元素的化合价为-2价 |
C、Na2O2的电子式为Na+ Na+ Na+ |
D、在MgO晶体中,O2-的结构示意图可表示为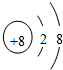 |
将钠、镁、铝各0.1mol分别放入500mL 1mol?L-1的盐酸中,同温同压下产生的气体体积比是( )
| A、1:2:3 |
| B、6:3:2 |
| C、3:1:1 |
| D、1:1:1 |
下列有关族的叙述正确的是( )
| A、IA族全是金属元素 |
| B、元素周期表中有7个主族,7个副族,一个0族,一个Ⅷ族 |
| C、元素周期表中第ⅡA族与第ⅢA族相邻 |
| D、所有族元素最外层电子数等于族序数 |
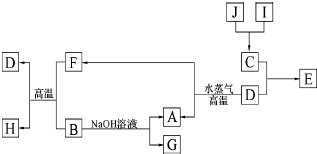
 科学家发现C60分子由60个碳原子构成,它的形状像足球(图丙),含有
科学家发现C60分子由60个碳原子构成,它的形状像足球(图丙),含有 键,因此又叫足球烯.1991年科学家又发现一种碳的单质--碳纳米管,是由六边环形的碳原子构成的具有很大表面积管状大分子(图丁),图甲、图乙分别是金刚石和石墨的结构示意图.图中小黑点均代表碳原子.
键,因此又叫足球烯.1991年科学家又发现一种碳的单质--碳纳米管,是由六边环形的碳原子构成的具有很大表面积管状大分子(图丁),图甲、图乙分别是金刚石和石墨的结构示意图.图中小黑点均代表碳原子.