题目内容
下列离子方程式中正确的是( )
| A、碳酸氢铵溶液与足量苛性钾溶液混合共热:NH4++OH-=NH3↑+H2O |
| B、Fe3O4溶解在过量的稀硝酸中:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| C、往硫酸铜溶液中加入过量的NaHS溶液:Cu2++2HS-=CuS↓+H2S↑ |
| D、石灰石溶解在醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.漏写碳酸氢根离子与碱的反应;
B.发生氧化还原反应生成硝酸铁和NO、水;
C.反应生成CuS、硫化氢和硫酸钠;
D.醋酸在离子反应中保留化学式.
B.发生氧化还原反应生成硝酸铁和NO、水;
C.反应生成CuS、硫化氢和硫酸钠;
D.醋酸在离子反应中保留化学式.
解答:
解:A.碳酸氢铵溶液与足量苛性钾溶液混合共热的离子反应为NH4++HCO3-+2OH-
NH3↑+CO32-+2H2O,故A错误;
B.Fe3O4溶解在过量的稀硝酸的离子反应为3Fe3O4+NO3-+28H+═9Fe3++14H2O+NO↑,故B错误;
C.往硫酸铜溶液中加入过量的NaHS溶液的离子反应为Cu2++2HS-=CuS↓+H2S↑,故C正确;
D.石灰石溶解在醋酸中的离子反应为CaCO3+2HAc=Ca2++H2O+CO2↑+2Ac-,故D错误;
故选C.
| ||
B.Fe3O4溶解在过量的稀硝酸的离子反应为3Fe3O4+NO3-+28H+═9Fe3++14H2O+NO↑,故B错误;
C.往硫酸铜溶液中加入过量的NaHS溶液的离子反应为Cu2++2HS-=CuS↓+H2S↑,故C正确;
D.石灰石溶解在醋酸中的离子反应为CaCO3+2HAc=Ca2++H2O+CO2↑+2Ac-,故D错误;
故选C.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及与量有关的离子反应考查,综合性较强,题目难度不大.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
用NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、1.0L 1.0mol?L-1 CH3COOH溶液中,CH3COOH分子数为NA |
| B、1mol Na2O2与足量H2O反应转移的电子数NA |
| C、常温常压下,22.4L氧气含有氧原子为2NA |
| D、1.8g重水(D2O)中,含有的质子数为0.1NA |
 有机物的结构可用“键线式”简化表示.如CH3-CH═CH-CH3可简写为
有机物的结构可用“键线式”简化表示.如CH3-CH═CH-CH3可简写为 .已知“瘦肉精”含有克伦特罗,其结构简式如图,下列有关克伦特罗的叙述不正确的是( )
.已知“瘦肉精”含有克伦特罗,其结构简式如图,下列有关克伦特罗的叙述不正确的是( )| A、该物质的分子式为C12H18ON2Cl2 |
| B、该物质分子中碳原子杂化方式有两种 |
| C、该物质的分子中有8种化学环境不同的氢原子 |
| D、该物质能发生的反应类型有:加成反应、酯化反应、氧化反应等 |
短周期元素X,Y,Z在周期表中的位置如图所示,则下列说法中错误的是( )
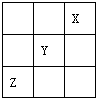

| A、X、Y、Z中X的单质最稳定 |
| B、Y的氢化物为HY |
| C、Z的最高价氧化物的化学式为ZO2 |
| D、能发生Cl2+H2Z═Z+2HCl的反应 |
若某电能与化学能的转化装置(电解池或原电池)中发生的总反应的离子方程式是Cu+2H+═Cu2++H2↑,则下列关于该装置的有关说法中正确的是( )
| A、该装置可能是原电池,可用Cu、C作电极,电解质溶液是盐酸 |
| B、该装置可能是原电池,电解质溶液为硝酸 |
| C、该装置只能是电解池,金属铜为该电解池的阳极,K2SO4为电解质溶液 |
| D、该装置只能是电解池,金属铜为该电解池的阳极,稀H2SO4为电解质溶液 |
下列各组微粒中,氧化性依次增强,且半径依次减小的是( )
| A、O、Cl、S、P |
| B、K+、Mg2+、Al3+、H+ |
| C、I-、Br-、Cl-、S2- |
| D、Al3+、Mg2+、Ca2+、Ba2+ |
在下列各溶液中,一定能大量共存的离子组是( )
| A、强酸性溶液中:K+、S2-、ClO-、SO42- |
| B、含有0.1mol?L-1 Fe3+的溶液中:K+、Mg2+、I-、NO3- |
| C、室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- |
| D、加入Al能放出H2的溶液中::Na+、K+、CO32-、Cu2+ |
