题目内容
下列说法正确的是( )
| A、金属钠着火可用煤油扑灭 |
| B、将几滴FeCl3饱和溶液滴入氢氧化钠溶液可制备Fe(OH)3胶体 |
| C、向含有等量NaI、NaCl的溶液中滴加AgNO3溶液,先产生白色沉淀 |
| D、用浓氢氧化钠溶液和湿润红色石蕊试纸检验某溶液中是否有NH4+ |
考点:钠的化学性质,胶体的重要性质,氯、溴、碘及其化合物的综合应用,常见阳离子的检验
专题:元素及其化合物
分析:A、煤油能燃烧.
B、Fe(OH)3胶体的制备是将饱和FeCl3溶液滴入沸水中;
C、根据同类型的沉淀,溶度积小的沉淀先析出来;
D、铵根离子和氢氧化钠溶液反应生成氨气,氨气能使湿润的红色石蕊试纸变蓝色.
B、Fe(OH)3胶体的制备是将饱和FeCl3溶液滴入沸水中;
C、根据同类型的沉淀,溶度积小的沉淀先析出来;
D、铵根离子和氢氧化钠溶液反应生成氨气,氨气能使湿润的红色石蕊试纸变蓝色.
解答:
解:A、煤油能燃烧,钠着火时使用煤油会使其燃烧更剧烈,故A错误;
B、Fe(OH)3胶体的制备具体方法为:将饱和FeCl3溶液逐滴滴入沸水中,继续煮沸至溶液呈红褐色,停止加热,故B错误;
C、同类型的沉淀,溶度积小的沉淀先析出,Ksp(AgCl)>Ksp(AgI),所以向含有等量NaI、NaCl的溶液中滴加AgNO3溶液,先产生黄色AgI沉淀,故C错误;
D、铵根离子和氢氧化钠溶液反应生成氨气,所以生成氨气需要氢氧化钠溶液,氨气能使湿润的红色石蕊试纸变蓝色,则需要红色石蕊试纸,故D正确.
故选D.
B、Fe(OH)3胶体的制备具体方法为:将饱和FeCl3溶液逐滴滴入沸水中,继续煮沸至溶液呈红褐色,停止加热,故B错误;
C、同类型的沉淀,溶度积小的沉淀先析出,Ksp(AgCl)>Ksp(AgI),所以向含有等量NaI、NaCl的溶液中滴加AgNO3溶液,先产生黄色AgI沉淀,故C错误;
D、铵根离子和氢氧化钠溶液反应生成氨气,所以生成氨气需要氢氧化钠溶液,氨气能使湿润的红色石蕊试纸变蓝色,则需要红色石蕊试纸,故D正确.
故选D.
点评:本题主要考查了物质的性质、用途与制备,掌握物质的性质是解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
对于苯乙烯(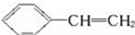 )的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )
)的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )
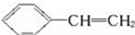 )的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )
)的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )| A、①②③⑤⑥ | B、①②⑤⑥ |
| C、①②④⑤ | D、①②③④⑤⑥ |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、0.1mol Fe在0.1mol Cl2中充分燃烧,转移的电子数为0.3NA |
| B、标准状况下,11.2L CCl4所含分子数约为0.5NA |
| C、常温下,pH=13的NaOH溶液中,OH-的数目为0.1NA |
| D、常温、常压下,14g CO与N2的混合气含的原子数为NA |
同浓度同体积的醋酸与盐酸相比,下列既能表明醋酸是弱酸,又能表明盐酸是强酸的是( )
| A、c(H+):盐酸大于醋酸 |
| B、盐酸中:c(H+)=c(Cl-),醋酸中:c(H+)<c(CH3COOH) |
| C、c(Cl-)>c(CH3COO-) |
| D、盐酸中:无氯化氢分子;醋酸中:存在大量醋酸分子 |
对于可逆反应H2(g)+I2(g)?2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是( )
| A、H2(g)的消耗速率与HI(g)的生成速率之比为2:1 |
| B、若平衡正向移动,则V正一定增大 |
| C、正、逆反应速率的比值是恒定的 |
| D、达到平衡时,正、逆反应速率相等 |
下列说法不正确的是( )
| A、人体缺碘会引起大脖子病,缺铁会引起贫血 |
| B、硅是构成一些岩石和矿物的基本元素 |
| C、NaHCO3受热易分解放出CO2,常用于制作糕点 |
| D、将Na2SO4分入钠盐和硫酸盐的分类方法属于树状分类法 |
Cl2是纺织工业中常用的漂白剂,Na2S2O3可作漂白布匹后的“脱氯剂”.脱氯反应为S2O32-+Cl2+H2O→SO42-+Cl-+H+(未配平).下列对该反应的说法不正确的是( )
| A、反应中硫元素发生了氧化反应 |
| B、脱氯反应后的溶液显酸性 |
| C、根据该反应可判断还原性:S2O32->Cl- |
| D、反应中每脱去1mol Cl2会生成1mol SO42- |