在一定温度下,在一体积不变的密闭容器中,反应2SO2(g)+O2(g)?2SO3(g)达到平衡状态的标志是( )
| A、单位时间内消耗n mol O2的同时生成2n mol SO3 |
| B、容器中的总压强不随时间的变化而改变 |
| C、容器中SO2、O2、SO3的物质的量比为2:1:2 |
| D、混合气体的密度保持不变 |
下列图象表达正确的是( )
A、 氨水的稀释 |
B、 等质量锌粉与足量盐酸反应 |
C、 氢气与氧气反应 中的能量变化 |
D、 气态氢化物沸点 |
两瓶NaCl溶液,一瓶NaCl溶液的物质的量浓度为c1 mol/L,密度为ρ1 g/mL;另一瓶NaCl溶液的物质的量浓度为c2 mol/L,密度为ρ2 g/mL,将它们等体积混合后,所得溶液的密度为ρ3 g/mL,则混合后NaCl溶液的物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
现有2mol/L的盐酸和氢氧化钠各100mL,分别加入等质量的铝粉,反应完全后,所产生的气体质量之比为2:3,则往酸中加入的铝粉的质量是( )
| A、2.7g | B、5.4g |
| C、8.1g | D、16.8g |
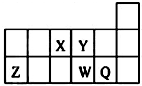 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法不正确的是( )
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法不正确的是( )| A、元素X与元素Z的最高正化合价之和的数值等于8 |
| B、Z的氧化物能与水反应 |
| C、离子Y2-和Z3+的核外电子数和电子层数都相同 |
| D、元素Y的氢化物的稳定性比W的氢化物强 |
下列物质中,既能与盐酸反应又能与NaOH溶液反应的是( )
①NaHCO3 ②Al(OH)3 ③Al2O3 ④(NH4)2SO3 ⑤Al.
①NaHCO3 ②Al(OH)3 ③Al2O3 ④(NH4)2SO3 ⑤Al.
| A、①② | B、②③⑤ |
| C、①②④⑤ | D、全部 |
 实验室中配制碘水,往往是将I2溶于KI溶液中,即可得到浓度较大的碘水,原因是发生了反应:I2(aq)+I-(aq)?I3-(aq).在上述反应的平衡体系中,I3-的物质的量浓度与温度T的关系如图所示(曲线上的任何一点都表示平衡状态).下列说法正确的是( )
实验室中配制碘水,往往是将I2溶于KI溶液中,即可得到浓度较大的碘水,原因是发生了反应:I2(aq)+I-(aq)?I3-(aq).在上述反应的平衡体系中,I3-的物质的量浓度与温度T的关系如图所示(曲线上的任何一点都表示平衡状态).下列说法正确的是( )| A、该反应的正反应为放热反应 |
| B、A状态与C状态的化学反应速率比较为v(A)>v(C) |
| C、在T1、D点状态时,v正<v逆 |
| D、由I2(aq)+I-(aq)?I3-(aq)推知,欲配制浓度较大的氯水,将氯气通入氯化钾溶液即可 |
 元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中Z的一种氧化物能使品红溶液褪色,则下列说法正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中Z的一种氧化物能使品红溶液褪色,则下列说法正确的是( )| A、非金属性:R<T<Q |
| B、T与Q的电子数相差18 |
| C、原子半径:R<T<Z |
| D、X的氧化物既能与盐酸反应又能与氢氧化钠溶液反应 |
某检测机构曾公布某公司生产的部分批次饮料产品游离余氯检测值超标.游离余氯超标可能是由于含氯处理水混入产品造成的,下列说法中正确的是( )
| A、游离余氯指的是Cl- |
| B、Cl-有害人体健康,含Cl-的饮料不能饮用 |
| C、游离余氯既不是电解质也不是非电解质 |
| D、游离余氯与水反应的生成物,对水的电离无影响 |