题目内容
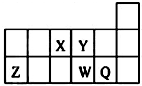 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法不正确的是( )
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法不正确的是( )| A、元素X与元素Z的最高正化合价之和的数值等于8 |
| B、Z的氧化物能与水反应 |
| C、离子Y2-和Z3+的核外电子数和电子层数都相同 |
| D、元素Y的氢化物的稳定性比W的氢化物强 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:这几种元素都是短周期元素,根据元素在周期表中位置知,X、Y、Z、W、Q分别是N、O、Al、S、Cl元素,
A.主族元素最高正化合价与其最外层电子数相等,但O、F元素除外;
B.Z的氧化物是氧化铝,和水不反应;
C.O原子得到2个电子生成O2-、Al原子失去3个电子生成Al3+;
D.元素的非金属性越强,其氢化物越稳定.
A.主族元素最高正化合价与其最外层电子数相等,但O、F元素除外;
B.Z的氧化物是氧化铝,和水不反应;
C.O原子得到2个电子生成O2-、Al原子失去3个电子生成Al3+;
D.元素的非金属性越强,其氢化物越稳定.
解答:
解:这几种元素都是短周期元素,根据元素在周期表中位置知,X、Y、Z、W、Q分别是N、O、Al、S、Cl元素,
A.X元素位于第VA族、Z元素为Al元素位于第IIIA族,所以X、Z元素最高正化合价为+5、+3,二者之和为8,故A正确;
B.Z的氧化物是氧化铝,氧化铝属于两性氧化物,能和强酸、强碱反应,但和水不反应,故B错误;
C.O原子得到2个电子生成O2-、Al原子失去3个电子生成Al3+,二者核外电子数都是10、电子层数都是2,所以氧离子、铝离子核外电子层数与核外电子数相等,故C正确;
D.非金属性Y>W,所以氢化物的稳定性Y>Z,故D正确;
故选B.
A.X元素位于第VA族、Z元素为Al元素位于第IIIA族,所以X、Z元素最高正化合价为+5、+3,二者之和为8,故A正确;
B.Z的氧化物是氧化铝,氧化铝属于两性氧化物,能和强酸、强碱反应,但和水不反应,故B错误;
C.O原子得到2个电子生成O2-、Al原子失去3个电子生成Al3+,二者核外电子数都是10、电子层数都是2,所以氧离子、铝离子核外电子层数与核外电子数相等,故C正确;
D.非金属性Y>W,所以氢化物的稳定性Y>Z,故D正确;
故选B.
点评:本题考查了元素周期表和元素周期律综合应用,根据原子结构、元素周期律等知识点分析解答,知道元素最高化合价与其族序数的关系、氢化物稳定性与非金属性强弱的关系,题目难度不大.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
化学与工农业生产、与人类生活都有密切相关,下列说法中正确的是( )
| A、14C可用于文物年代的鉴定,14C与12C互为同素异形体 |
| B、葡萄糖注射液不能产生丁达尔效应现象,不属于胶体 |
| C、汽油、柴油和植物油都是碳氢化合物 |
| D、“春蚕到死丝方尽,蜡烛成灰泪始干”中的“丝”和“泪”分别是指纤维素和油脂 |
2008年诺贝尔化学奖得主钱永健16岁时就以研究金属与硫氰化合物结合而获得“西屋科学天才奖”.根据所学知识,下列离子在溶液中易与SCN -结合的是( )
| A、K+ |
| B、NH4+ |
| C、Na+ |
| D、Fe3+ |
 原子序数为16的元素E在周期表中位于A、B、C、D四种元素中间(如图所示),则下列说法错误的是( )
原子序数为16的元素E在周期表中位于A、B、C、D四种元素中间(如图所示),则下列说法错误的是( )| A、A元素的最高价氧化物为P2O5 |
| B、C元素原子核外有17个电子 |
| C、B元素的原子序数为8 |
| D、D元素的原子序为为24 |
下列叙述正确的是( )
| A、自来水用氯气消毒是因为氯气有毒,可毒死细菌、病毒 |
| B、道尔顿的原子学说存在缺陷和错误,因而意义不大 |
| C、焙制糕点时的发酵粉以小苏打为主要成分 |
| D、做焰色反应时,蘸取样品之前需用氢氧化钠溶液清洗铂丝 |
在一定温度下,在一体积不变的密闭容器中,反应2SO2(g)+O2(g)?2SO3(g)达到平衡状态的标志是( )
| A、单位时间内消耗n mol O2的同时生成2n mol SO3 |
| B、容器中的总压强不随时间的变化而改变 |
| C、容器中SO2、O2、SO3的物质的量比为2:1:2 |
| D、混合气体的密度保持不变 |
下列说法中正确的是( )
| A、摩尔是国际单位制中的七个物理量之一 |
| B、摩尔是物质的量的单位,简称摩,符号为mol |
| C、氧气的摩尔质量为32g |
| D、每摩尔任何物质均含有6.02×1023个原子 |
下列各组离子在指定溶液中一定能大量共存的是( )
| A、水电离的c(H+)=1×10-13mol/L的溶液中:Na+、Ba2+、Cl-、NO3- |
| B、使酚酞变红色的溶液:Na+、Cu2+、HCO3-、NO3- |
| C、在酸性条件下:Fe2+、Cl-、NO3-、K+ |
| D、在无色溶液中:Al3+、Cl-、K+、AlO2- |