将物质的量浓度都是0.1mol?L-1的某弱酸HX溶液与NaX溶液等体积混合,下列说法错误的是( )
| A、若混合后溶液中c(Na+)>c(X-),说明HX的电离程度弱于X-的水解程度 |
| B、若混合溶液呈酸性,则c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-) |
| C、混合溶液中c(HX)+c(X-)=0.2mol?L-1 |
| D、混合溶液中c(HX)+c(X-)=2c(Na+) |
伞形酮可由雷梭苯乙酮和苹果酸在一定条件下反应值得
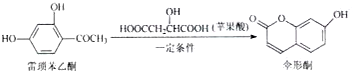
下列有关这三种物质的说法错误的是( )

下列有关这三种物质的说法错误的是( )
| A、雷梭苯乙酮有两种含氧官能团 |
| B、苹果酸和伞形酮分子中均含有1个手性碳原子 |
| C、雷梭苯乙酮和伞形酮都能跟FeCl3溶液发生显色反应 |
| D、1mol伞形酮与足量NaOH溶液反应,最多可消耗2mol NaOH |
化学与生产、生活密切相关.下列说法正确的是( )
| A、汽车尾气的排放是雾霾形成的重要原因之一 |
| B、“玉兔”月球车太阳能电池帆板的材料是二氧化硅 |
| C、酒精能使蛋白质变性,医疗上常用无水酒精作消毒剂 |
| D、地沟油可用作汽车燃料,其组成与汽油、煤油、柴油相同 |
已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ/mol,相关数据如下
一定条件下,在体积为1L的密闭容器中加入1molN2和3molH2充分反应,放出热量Q1kJ,下列说法正确的是( )
| H2(g) | N2(g) | NH3(g) | |
| 1mol分子中的化学键形成时要释放出的能量/kJ | 436 | 946 | a |
A、如图可表示合成氨过程中的能量变化 |
| B、a的数值为391 |
| C、Q1的数值为92 |
| D、相同条件下,反应物若为2molN2和6molH2,放出热量Q2>2Q1 |
镁燃料电池以镁合金作为电极的一极,另一极充入过氧化氢,电解质是酸化的氯化钠溶液,放电时总反应为:Mg+2H++H2O2=Mg2++2H2O,关于该电池的说法不正确的是( )
| A、镁合金为电源负极,发生氧化反应 |
| B、电解质溶液中的H+向正极移动 |
| C、正极反应为:H2O2+2e-=2OH- |
| D、放电时正极周围溶液的pH升高 |
下列食用物质中,热值最高的是( )
| A、酒精 | B、葡萄糖 |
| C、油脂 | D、蛋白质 |
在2p能级上最多只能排布6个电子,其依据的规律是( )
| A、能量最低原理 |
| B、泡利不相容原理 |
| C、洪特规则 |
| D、能量最低原理和泡利不相容原理 |
下列说法正确的是( )
| A、浓硫酸有氧化性,稀硫酸没有氧化性 |
| B、CO2和SO2都是酸性氧化物,与NaOH溶液反应均可生成两种盐 |
| C、常温下浓硝酸和稀硝酸均可用铁质容器盛装 |
| D、澄清石灰水可用来鉴别Na2CO3和NaHCO3溶液 |
下列离子在溶液中可以大量共存的是( )
| A、Na+、Ca2+、OH-、CO32- |
| B、Al3+、H+、Cl-、SO42- |
| C、Fe3+、H+、NO3-、SO42- |
| D、Na+、H+、SO32-、ClO- |
已知某密闭容器中发生反应:X(g)+2Y(g)?W(g)+Z(g),△H<0(Y物质极易被熔化),下列说法一定正确的是( )
| A、若W为有颜色的物质,达到平衡后,增大压强,体系颜色变浅 |
| B、改变压强但不改变温度,该反应平衡常数不变 |
| C、平衡时,其它条件不变,升高温度,正反应速率增大程度比逆反应率增大程度小 |
| D、平衡时,其它条件不变,分离出Z,正反应速率加快 |