下列表达方式不正确的是( )
A、二氧化碳的电子式是 | ||
B、氟化钠的电子式  | ||
C、S2-离子的结构示意图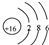 | ||
D、镁-24原子
|
常温下,取浓度相同的NaOH和HCl溶液,以3:2体积比相混合,所得溶液的pH等于13,则原溶液的浓度为 ( )
| A、0.1 mol?L-1 |
| B、0.7 mol?L-1 |
| C、0.5 mol?L-1 |
| D、1.0 mol?L-1 |
下列操作完成后,没有沉淀的是( )
| A、向Ca( OH)2与FeCl2混合溶液加足量稀HNO3 |
| B、向Ba( OH)2与KNO3混合溶液加足量稀H2SO4 |
| C、向AgNO3与Na2CO3混合溶液加足量稀HCl |
| D、向BaCl2与Na2CO3混合溶液中加足量AgNO3溶液 |
下列关于Cl2和Cl-的说法中,正确的是( )
| A、都有毒 |
| B、都属于同一元素 |
| C、都呈黄绿色 |
| D、都能和钠反应 |
在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的有( )
| A、滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、S2- |
| B、pH值为1的溶液:Cu2+、K+、Mg2+、NO3- |
| C、水电离出来的c(H+)=10-13mol/L的溶液:Na+、HCO3-、Br-、Ba2+ |
| D、所含溶质为Na2CO3的溶液:K+、SO42-、NO3-、Al3+ |
下列叙述正确的是( )
| A、SO2能使溴水、酸性高锰酸钾溶液退色是因为SO2有漂白性 |
| B、若将SO2和Cl2以等物质的量混合后通入品红溶液中一定退色更快 |
| C、SO2通入Ba(OH)2溶液中,有白色沉淀生成,加入稀硝酸最终沉淀全部溶解 |
| D、SO2通入BaCl2溶液中无沉淀生成 |
 参照反应Br+H2?HBr+H的能量对反应历程的示意图(如图),下列叙述中正确的是( )
参照反应Br+H2?HBr+H的能量对反应历程的示意图(如图),下列叙述中正确的是( )| A、加入催化剂,该化学反应的反应热变大 |
| B、正反应为吸热反应 |
| C、正反应为放热反应 |
| D、正反应的反应热为△H1 |
绿原酸的结构简式如图所示,下列有关绿原酸的叙述不正确的是( )


| A、绿原酸的分子式为C16H18O9 |
| B、一定不能使Na2CO3溶液放出气体 |
| C、0.5mol绿原酸最多与2mol NaOH反应 |
| D、能发生取代反应,加成反应和消去反应 |
已知部分钡盐的溶度积如下:Ksp(BaCO3)=8.1×10-9,Ksp[Ba(IO3)2]=6.5×10-10,Ksp(BaSO4)=1.1×10-10,Ksp(BaCrO4)=1.6×10-10.一种溶液中存在相同浓度的CO32-、CrO42-、IO3-、SO42-,且浓度均为0.001mol/L,若向该溶液中逐滴滴入BaCl2溶液,首先发生的离子方程式为( )
| A、Ba2++CO32-═BaCO3↓ |
| B、Ba2++CrO42-═BaCrO4↓ |
| C、Ba2++2IO3-═Ba(IO3)2↓ |
| D、Ba2++SO42-═BaSO4↓ |
下列物质转化在给定条件下能实现的是( )
A、N2
| ||||
B、NaCl(aq)
| ||||
C、Fe3O4
| ||||
D、Al2(SO4)
|