题目内容
下列叙述正确的是( )
| A、SO2能使溴水、酸性高锰酸钾溶液退色是因为SO2有漂白性 |
| B、若将SO2和Cl2以等物质的量混合后通入品红溶液中一定退色更快 |
| C、SO2通入Ba(OH)2溶液中,有白色沉淀生成,加入稀硝酸最终沉淀全部溶解 |
| D、SO2通入BaCl2溶液中无沉淀生成 |
考点:二氧化硫的化学性质
专题:氧族元素
分析:A.SO2与溴水、酸性高锰酸钾溶液均发生氧化还原反应;
B.SO2和Cl2以等物质的量混合,在水中反应生成硫酸和盐酸;
C.二氧化硫为酸性氧化物,亚硫酸钡能被硝酸氧化生成硫酸钡;
D.盐酸的酸性大于亚硫酸.
B.SO2和Cl2以等物质的量混合,在水中反应生成硫酸和盐酸;
C.二氧化硫为酸性氧化物,亚硫酸钡能被硝酸氧化生成硫酸钡;
D.盐酸的酸性大于亚硫酸.
解答:
解:A.SO2与溴水、酸性高锰酸钾溶液均发生氧化还原反应,使其褪色,与二氧化硫的还原性有关,与漂白性无关,故A错误;
B.SO2和Cl2以等物质的量混合,在水中反应生成硫酸和盐酸,不具有漂白性,则通入品红溶液中,颜色不变,故B错误;
C.二氧化硫为酸性氧化物,亚硫酸钡能被硝酸氧化生成硫酸钡,则SO2通入Ba(OH)2溶液中,有白色沉淀生成,加入稀硝酸生成硫酸钡沉淀,不能溶解,故C错误;
D.盐酸的酸性大于亚硫酸,则SO2通入BaCl2溶液中,不发生反应,无沉淀生成,故D正确;
故选D.
B.SO2和Cl2以等物质的量混合,在水中反应生成硫酸和盐酸,不具有漂白性,则通入品红溶液中,颜色不变,故B错误;
C.二氧化硫为酸性氧化物,亚硫酸钡能被硝酸氧化生成硫酸钡,则SO2通入Ba(OH)2溶液中,有白色沉淀生成,加入稀硝酸生成硫酸钡沉淀,不能溶解,故C错误;
D.盐酸的酸性大于亚硫酸,则SO2通入BaCl2溶液中,不发生反应,无沉淀生成,故D正确;
故选D.
点评:本题考查二氧化硫的性质,为高频考点,把握二氧化硫的还原性、漂白性及酸性氧化物性质为解答的关键,注意C中的氧化还原反应及D中酸性比较,题目难度中等.

练习册系列答案
相关题目
如图是元素周期表短周期的一部分.其中F原子的电子层数为n,最外层电子数为2n+1,核内质子数为2n2-1.下列说法不正确的是( )
| A | B | C | |
| D | E | F |
| A、D的单质是常见的半导体材料 |
| B、B与E形成的化合物不只一种 |
| C、C与F的原子序数之差一定为8 |
| D、C属于卤族元素,对应的单质能与水反应生成两种酸 |
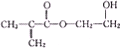 甲基丙烯酸烃乙酯是一种有机合成中重要的原料,其结构简式如图所示,下列有关说法错误的是( )
甲基丙烯酸烃乙酯是一种有机合成中重要的原料,其结构简式如图所示,下列有关说法错误的是( )| A、能发生加成反应 |
| B、能发生取代反应 |
| C、一定条件下,能与乙醇发生酯化反应 |
| D、既能是溴水褪色,又能使酸性高猛酸钾溶液褪色 |
NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
| A、含0.1mol BaCl2的溶液中Cl-数为0.2NA |
| B、22g CO2所含有的分子数为0.5NA 已知M(CO2)=44g/mol |
| C、11.2L CO2所含有的分子数为0.5NA |
| D、常温下NA个N2分子电子数为14NA |
已知同周期的X、Y、Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序为HZO4>H2YO4>H3XO4,下列说法中正确的是( )
| A、三种元素的原子序数按Z、Y、X的顺序增大 |
| B、单质的氧化性按X、Y、Z的顺序减弱 |
| C、原子半径按X、Y、Z的顺序增大 |
| D、气态氢化物的稳定性按X、Y、Z的顺序增强 |
下列表达方式不正确的是( )
A、二氧化碳的电子式是 | ||
B、氟化钠的电子式  | ||
C、S2-离子的结构示意图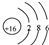 | ||
D、镁-24原子
|
在标准状况下,相同质量的下列气体体积最大的是( )
| A、CH4 |
| B、O2 |
| C、Cl2 |
| D、CO2 |
元素周期律的发现对新元素的发现、化学理论和实验等研究工作起到了指导作用.周期律揭示的规律包括以下内容中的( )
①元素的性质随原子序数的递增呈周期性变化
②元素的性质是元素原子序数的周期性函数
③事物的量变可以引起质变
④元素性质的递变是原子核外电子排布的必然结果.
①元素的性质随原子序数的递增呈周期性变化
②元素的性质是元素原子序数的周期性函数
③事物的量变可以引起质变
④元素性质的递变是原子核外电子排布的必然结果.
| A、①② | B、①③ |
| C、①④ | D、①②③④ |
设阿伏加德罗常数的值为NA,下列叙述正确的是( )
A、常温下,1L 0.1mol?L-1的NH4NO3溶液中NH
| ||
| B、常温下,4.4g CO2和N2O混合物中所含有的原子数为0.3NA | ||
| C、标准状况下,2.24L乙烷中含有的非极性键数为0.7NA | ||
| D、1molCl2与足量的氢氧化钠溶液反应转移的电子数为2NA |