题目内容
下列表达方式不正确的是( )
A、二氧化碳的电子式是 | ||
B、氟化钠的电子式  | ||
C、S2-离子的结构示意图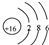 | ||
D、镁-24原子
|
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.二氧化碳分子中存在两个碳氧双键,碳原子和氧原子最外层达到8电子稳定结构;
B.氟化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,氟离子还需要标出最外层电子;
C.硫离子的核外电子总数为18,最外层为8个电子;
D.镁-24原子的核电荷数为12、质量数为24.
B.氟化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,氟离子还需要标出最外层电子;
C.硫离子的核外电子总数为18,最外层为8个电子;
D.镁-24原子的核电荷数为12、质量数为24.
解答:
解:A.二氧化碳属于共价化合物,分子中存在两个碳氧双键,二氧化碳的电子式为: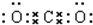 ,故A正确;
,故A正确;
B.氟化钠为离子化合物,钠离子直接用离子符号表示,氟离子需要标出电荷及最外层电子,氟化钠的电子式为: ,故B正确;
,故B正确;
C.硫离子的核电荷数为16,最外层为8个电子,硫离子正确的结构示意图为: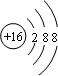 ,故C错误;
,故C错误;
D.镁-24原子的质子数为12、质量数为24,则该原子可以表示为:
Mg,故D正确;
故选C.
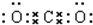 ,故A正确;
,故A正确;B.氟化钠为离子化合物,钠离子直接用离子符号表示,氟离子需要标出电荷及最外层电子,氟化钠的电子式为:
 ,故B正确;
,故B正确;C.硫离子的核电荷数为16,最外层为8个电子,硫离子正确的结构示意图为:
 ,故C错误;
,故C错误;D.镁-24原子的质子数为12、质量数为24,则该原子可以表示为:
24 12 |
故选C.
点评:本题考查了电子式、离子结构示意图、元素符号的表示方法判断,题目难度中等,注意掌握常见化学用语的概念及正确的表示方法,明确离子结构示意图与原子结构示意图、离子化合物与共价化合物的电子式的区别.

练习册系列答案
相关题目
在室温下,下列有关电解质溶液叙述中错误的是( )
A、若某溶液中
| ||
| B、10mL 0.02mol/L HCl溶液与10mL 0.02mol/L Ba(OH)2溶液充混合,若混合后溶液的体积为20mL,则溶液的pH=12 | ||
| C、将一定体积的稀盐酸与稀氨水相混合,当溶质为NH3?H2O和NH4Cl时溶液pH≥7 | ||
| D、向Na2CO3溶液中逐滴滴加盐酸至过量时,溶液中c(HCO3-)的变化情况是先变大后变小 |
镭是元素周期表中第七周期的ⅡA族元素.下面关于镭的性质的描述中不正确的是( )
| A、价层电子构型为7S2 |
| B、单质能与冷水反应,放出氢气 |
| C、氢氧化物呈两性 |
| D、碳酸盐难溶于水 |
以下能级符号正确的是( )
| A、3f | B、1p | C、2d | D、4s |
下列叙述正确的是( )
| A、SO2能使溴水、酸性高锰酸钾溶液退色是因为SO2有漂白性 |
| B、若将SO2和Cl2以等物质的量混合后通入品红溶液中一定退色更快 |
| C、SO2通入Ba(OH)2溶液中,有白色沉淀生成,加入稀硝酸最终沉淀全部溶解 |
| D、SO2通入BaCl2溶液中无沉淀生成 |
我省盛产矿盐(主要成分是NaCl,还含有SO42-等其他可溶性杂质的离子).下列有关说法正确的是( )
| A、有矿盐生成食盐,除去SO42- 最合适的实际是Ba(NO3)2 |
| B、工业上通过电解氯化钠溶液制备金属钠和氯气 |
| C、用酚酞试液可鉴别饱和食盐水和饱和纯碱溶液 |
| D、室温下,AgCl在水中的溶解度小于在食盐中的溶解度 |
下列离子方程式正确的是( )
| A、氯气溶于水:Cl2+H2O═2H++Cl-+ClO- |
| B、铝粉没入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
| C、铁与盐酸反应:Fe+2H+═Fe3++H2↑ |
| D、Ba(OH)2与稀H2SO4反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A、24g NaH中阴离子所含电子总数为NA |
| B、1mol苯分子中含有3NA个碳碳单键 |
| C、NO2和H2O反应毎生成2mol HNO3时转移的电子数目为2NA |
| D、含0.2 NA个K+的K2SO4固体溶解于1 L水中,所得溶液浓度为0.1mol?L-1 |
下列电子式书写正确的是( )
A、氯化钠 |
B、氨气 |
C、氯化钙 |
D、硫化钠 |