下列事实不能用勒夏特列原理解释的是( )
| A、将氯化铁溶液加热蒸干最终得不到氯化铁固体 |
| B、实验室中常用排饱和食盐水的方法收集氯气 |
| C、开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| D、钢铁在潮湿的空气中生锈 |
在一定温度下的容积不变的密闭容器中,下列叙述不是可逆反应A(g)+3B(g)?2C(g)+2D(s)达到平衡的标志的是( )
①C的生成速率与C的消耗速率相等
②单位时间内生成amolA,同时生成3amolB
③A、B、C的浓度不再改变
④混合气体的密度不再改变
⑤混合气体的总压强不再改变
⑥混合气体的总物质的量不再改变
⑦A、B、C、D浓度之比为1:3:2:2.
①C的生成速率与C的消耗速率相等
②单位时间内生成amolA,同时生成3amolB
③A、B、C的浓度不再改变
④混合气体的密度不再改变
⑤混合气体的总压强不再改变
⑥混合气体的总物质的量不再改变
⑦A、B、C、D浓度之比为1:3:2:2.
| A、②⑦ | B、②⑤⑦ |
| C、①③④⑦ | D、②⑤⑥⑦ |
常温常压下,下列各组物质中,原子数一定相同的是( )
| A、14g N2和32g O2 |
| B、11.2L O2和0.5mol O2 |
| C、2L CO2和2L H2O |
| D、17g NH3和4g H2 |
对于有气体参加的反应,一定能使化学反应速率加快的因素是( )
①扩大容器的容积 ②使用催化剂 ③增加反应物的物质的量 ④升高温度 ⑤缩小容积 ⑥增大容器内的压强.
①扩大容器的容积 ②使用催化剂 ③增加反应物的物质的量 ④升高温度 ⑤缩小容积 ⑥增大容器内的压强.
| A、②③ | B、②③④⑥ |
| C、②③④⑤ | D、②④ |
右图为阳离子交换膜法电解饱和食盐水原理示意图,下列说法不正确的是( )

| A、从E口逸出的气体是H2 |
| B、从B口加入含少量NaOH的水溶液以增强导电性 |
| C、标准状况下每生成22.4 LCl2,便产生2 mol NaOH |
| D、电解一段时间后加适量盐酸可以恢复到电解前的浓度 |
在标准状况下,由0.5gH2、11g CO2和4g O2组成的混合气体,其体积约为( )
| A、8.4L | B、11.2L |
| C、14.0L | D、16.8L |
如图分别表示四种操作,其中至少有两处错误的是( )
A、 读数 |
B、 称量 |
C、 溶解 |
D、 |
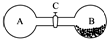 如图所示,容器A(容积2L)中有1×105 Pa的空气.在容器B(容积1L)中放入少量的只吸附氧气的吸附剂,保持真空.打开旋塞C,放置片刻,容器内的总压强变为0.6×105 Pa,这时气体中氮气和氧气的分子数之比最接近的数值是(吸附剂的体积可忽略不计)
如图所示,容器A(容积2L)中有1×105 Pa的空气.在容器B(容积1L)中放入少量的只吸附氧气的吸附剂,保持真空.打开旋塞C,放置片刻,容器内的总压强变为0.6×105 Pa,这时气体中氮气和氧气的分子数之比最接近的数值是(吸附剂的体积可忽略不计)( )
| A、8:1 | B、10:1 |
| C、12:1 | D、14:1 |
NA代表阿伏加德罗常数,下列叙述正确的是( )
| A、50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
| B、常温常压下,48 gO2和O3的混合气体中含有的氧原子数为3NA |
| C、在标准状况下,11.2L O2和22.4 L NO混合并充分反应后得到的气体分子数为NA |
| D、常温下5.6克铁投入到足量浓硝酸中反应,转移电子数为0.3NA |
NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、1L0.1 mol?L-1 盐酸中含NA个HCl分子 |
| B、常温常压下,22.4L NH3含4NA个原子 |
| C、常压、4℃,18mLH2O中含有10NA个电子 |
| D、标准状况下,64 g SO2所含分子数为NA个 |