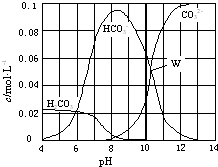
 25℃时,0.1mol Na2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH 的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )
25℃时,0.1mol Na2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH 的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )| A、W点所示的溶液中:c(CO32-)=c(HCO3-)>c(OH-)>c(H+) |
| B、pH=4的溶液中:c(H2CO3)+c(HCO3-)+c(CO32-)=0.1mol?L-1 |
| C、pH=8的溶液中:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) |
| D、pH=11的溶液中:c(Na+)+c (H+)=c(OH-)+c(Cl-)+c(CO32-)+c(HCO3-) |
下列离子方程式书写正确的是( )
| A、二氧化锰与浓盐酸共热:MnO2+4H++2Cl-═Mn2++Cl2↑+2H2O |
| B、向次氯酸钙溶液中通入过量的CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO |
| C、氯气通入水中:Cl2+H2O═2H++Cl-+ClO- |
| D、铜与稀硝酸反应:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、在常温常压下,11.2L O2含有的原子数为0.5NA |
| B、标准状况下,22.4L H2O所含的分子数为NA |
| C、质量为23g的两块钠和足量O2反应分别生成Na2O2和Na2O,转移的电子数都为NA |
| D、2L 0.3mol/L Na2SO4溶液中含0.6NA个Na+ |
下列叙述中,正确的是( )
| A、熔融态不导电,水溶液能导电的电解质一定是弱电解质 |
| B、常温下0.1mol?L-1氨水溶液的pH=a,将溶液稀释到原体积的10倍 后溶液pH=(a-1) |
| C、25℃时,将一定量冰醋酸加水稀释,溶液导电能力不一定减小 |
| D、向HF溶液中不断加水,溶液中所有离子浓度均减小 |
常温下列各种溶液中,可能大量共存的离子组是( )
| A、pH=0的溶液中:Fe2+、NO3-、SO42-、I- |
| B、由水电离出的c(H+)=1×10-13mol?L-1的溶液中:Na+、AlO2-、S2-、CO32- |
| C、含有大量Fe3+的溶液中:Na+、I-、K+、NO3- |
| D、能使pH试纸显红色的溶液:Mg2+、SO42-、Na+、Cl- |
下列离子方程式中,正确的是( )
| A、铁与盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
| B、氯气与氯化亚铁溶液反应:2FeCl2+Cl2═2FeCl3 |
| C、氯化铁溶液与铁反应:Fe3++Fe═2Fe2+ |
| D、氯化铁溶液与氢氧化钠溶液反应:Fe3++3OH-═Fe(OH)3↓ |
下列变化中,属于还原反应的是( )
| A、Fe→FeSO4 |
| B、Cu(NO3)2→Cu |
| C、P→P2O5 |
| D、NaCl→AgCl |
下列数字表示元素的原子序数,其中包含金属、非金属、稀有气体元素各一种的是( )
| A、3、16、20 |
| B、2、4、18 |
| C、11、15、18 |
| D、9、10、17 |
在三个密闭容器中分别充入CO、CH4、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是( )
| A、p(CO)>p(CH4)>p(O2) |
| B、p(O2)>p(CO)>p(CH4) |
| C、p(CH4)>p(O2)>p(CO) |
| D、p(CH4)>p(CO)>p(O2) |
下列描述或化学用语书写错误的是( )
| A、向Fe(OH)3胶体中滴加稀硫酸,先生成红褐色沉淀,后沉淀逐渐溶解 |
| B、向铜粉中加入稀硫酸,铜粉不溶解,再加入硝酸钾固体,铜粉逐渐溶解 |
| C、向明矾(KAl(SO4)2?12H2O)溶液中滴入Ba(OH)2溶液,SO42-恰好完全沉淀时的离子方程式为:Ba2++3OH-+Al3++SO42-═BaSO4↓+Al(OH)3↓ |
| D、氯碱工业和金属钠的冶炼都用到了NaCl,阳极上发生的电极反应都是:2Cl-+2e-=Cl2↑ |