题目内容
下列离子方程式中,正确的是( )
| A、铁与盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
| B、氯气与氯化亚铁溶液反应:2FeCl2+Cl2═2FeCl3 |
| C、氯化铁溶液与铁反应:Fe3++Fe═2Fe2+ |
| D、氯化铁溶液与氢氧化钠溶液反应:Fe3++3OH-═Fe(OH)3↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.反应生成氯化亚铁和氢气;
B.反应生成氯化铁,氯化亚铁、氯化铁均电离;
C.电子、电荷不守恒;
C.反应生成氢氧化铁和氯化钠.
B.反应生成氯化铁,氯化亚铁、氯化铁均电离;
C.电子、电荷不守恒;
C.反应生成氢氧化铁和氯化钠.
解答:
解:A.铁与盐酸反应的离子反应为Fe+2H+═Fe2++H2↑,故A错误;
B.氯气与氯化亚铁溶液反应的离子反应为2Fe2++Cl2═2Fe3++2Cl-,故B错误;
C.氯化铁溶液与铁反应的离子反应为2Fe3++Fe═3Fe2+,故C错误;
D.氯化铁溶液与氢氧化钠溶液反应的离子反应为Fe3++3OH-═Fe(OH)3↓,故D正确;
故选D.
B.氯气与氯化亚铁溶液反应的离子反应为2Fe2++Cl2═2Fe3++2Cl-,故B错误;
C.氯化铁溶液与铁反应的离子反应为2Fe3++Fe═3Fe2+,故C错误;
D.氯化铁溶液与氢氧化钠溶液反应的离子反应为Fe3++3OH-═Fe(OH)3↓,故D正确;
故选D.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,注意电子、电荷守恒的应用,题目难度不大.

练习册系列答案
相关题目
抗酸药中既能与强酸反应,又能与强碱反应,又能适应胃溃疡病人的物质是( )
| A、CaCO3 |
| B、Al(OH)3 |
| C、Mg(OH)2 |
| D、NaHCO3 |
下列变化属于物理变化的是( )
| A、水沸腾产生大量水蒸气 |
| B、木材燃烧 |
| C、钢铁生锈 |
| D、黑火药爆炸 |
向一个密闭的容器中充入SO2与18O2,加入适当的催化剂并加热到一定的温度使之发生反应,反应一段时间后,18O会存在于( )
| A、SO2中 |
| B、SO2和SO3中 |
| C、SO2和O2中 |
| D、SO2、SO3和O2中 |
下列溶液中的Cl-浓度与50ml1mol/l的氯化铝溶液中的氯离子浓度相等的是( )
| A、150ml 1mol/l NaCl |
| B、75m l2mol/l NH4Cl |
| C、150ml 3mol/lKCl |
| D、75ml 1mol/l CaCl2 |
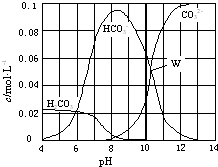 25℃时,0.1mol Na2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH 的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )
25℃时,0.1mol Na2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH 的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )| A、W点所示的溶液中:c(CO32-)=c(HCO3-)>c(OH-)>c(H+) |
| B、pH=4的溶液中:c(H2CO3)+c(HCO3-)+c(CO32-)=0.1mol?L-1 |
| C、pH=8的溶液中:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) |
| D、pH=11的溶液中:c(Na+)+c (H+)=c(OH-)+c(Cl-)+c(CO32-)+c(HCO3-) |
关于SO2 的叙述中,正确的是( )
| A、SO2 的摩尔质量是64 g |
| B、常温常压下,64 g SO2 中所含的分子数为6.02×1023 个 |
| C、1 mol SO2 的质量是64 g/mol |
| D、常温常压下,1 mol SO2 的体积为22.4 L |