如图为浓度各为0.1mol/L的酸HA和碱BOH的溶液中,溶质分子浓度随pH值的改变而变化的情况.下列说法中不正确的是( )
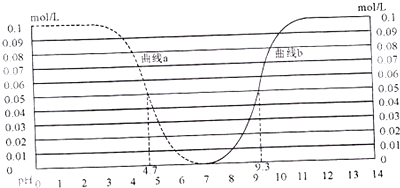

| A、曲线a代表酸HA,曲线b代表碱BOH | ||
B、在0.1mol/L的BOH溶液中,但溶液的pH从8逐渐变为11时,
| ||
| C、在0.1mol/L的NaA溶液中,若通过加少量纯HA改变溶液pH时,一定有:c(Na+)-c(OH-)=c(A-)-c(H+) | ||
| D、用等物质的量浓度的NaOH溶液和盐酸分别滴定等浓度等体积的酸HA和BOH溶液时,所消耗的NaOH溶液和盐酸的体积相同 |
下列颜色变化与氧化还原反应无关的是( )
| A、将乙醇滴入酸性K2Cr2O7溶液中,溶液由橙色变为绿色 |
| B、将SO2通入滴有酚酞的NaOH溶液中,溶液红色褪去 |
| C、将H2C2O4溶液滴入酸性KMnO4溶液中,溶液紫色褪去 |
| D、将乙醛加入新制Cu(OH)2悬浊液中并加热至沸腾,出现红色沉淀 |
化合物分子中原子(或原子团)间的相互影响会导致化学性质的不同,下列叙述不能说明这一点的是( )
| A、Na与水反应比与C2H5OH反应强烈 |
| B、丙酮(CH3COCH3)分子中的氢原子比乙烷分子中的氢原子更易被卤素原子取代 |
| C、甲酸的酸性比乙酸强 |
| D、相等质量的甲醇和乙醇分别与足量金属钠反应,甲醇产生的H2更多 |
下列实验事实的描述中,正确的是( )
| A、实验室用加热分解氯化铵的方法制氨气 |
| B、向浓硫酸中缓慢加入乙醇和冰醋酸用以制备乙酸乙酯 |
| C、向2mL 10% NaOH溶液中,加入2mL 2mol/L CuSO4溶液,振荡制Cu(OH)2悬浊液,用于检验醛的性质 |
| D、加入Mg(OH)2固体可除去MgCl2溶液中混有的少量FeCl3 |
煤化工的产品很多,如合成气(CO、H2)、甲醇等对煤炭工业转型具有重要意义.下列说法不正确的是( )
| A、煤转化为气态燃料,可以降低碳的排放 |
| B、甲醇的沸点是64.5℃,甲醇中的水分可采用蒸馏法分离 |
| C、工业上利用饱和的K2CO3溶液分离回收废气中的CO2,符合低碳经济理念 |
| D、采用内衬聚四氟乙烯的钢管输送合成气,可有效减缓钢管的腐蚀 |
下列说法不正确的是( )
| A、纸上层析法通常以滤纸作为惰性支持物,滤纸纤维上的羟基具有亲水性,它所吸附的水作固定相 |
| B、用移液管取25.00mL液体于锥形瓶中时不得将移液管下端深入锥形瓶内 |
| C、实验中不慎将苯酚沾到皮肤上,应立即用酒精洗涤,再用水冲洗 |
| D、将3~4个火柴头浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸和NaNO2溶液,若出现白色沉淀,说明含有氯元素 |
用如图装置电解硫酸钾溶液制取氢气,氧气,硫酸和氢氧化钾.从开始通电时,收集B和C逸出的气体.1min后测得B口的气体体积为C口处的一半,下列说法不正确的是( )

| A、电源左极为正极 |
| B、电解槽左侧的电极反应方程式为:2H2O-4e-═O2+4H+ |
| C、D口导出的溶液为KOH溶液,且浓度比刚加入电解槽右侧时的浓度大 |
| D、在标准状况下,若1min后从C口处收集到的气体比B口处收集到的气体多2.24L,则有0.1NA个SO42-通过阴离子膜 |
下列各选项所描述的两个量中,前者一定大于后者的是( )
| A、pH=3的盐酸的Cl-浓度和pH=3的醋酸溶液的CH3COO-浓度 |
| B、pH相同的氨水和醋酸钠溶液中,由水电离产生的c(H+) |
| C、0.1mol/L的盐酸和0.1mol/L的醋酸分别与金属镁反应的速率 |
| D、pH=11的NaOH和pH=11的氨水分别稀释100倍后的pH |
下列实验能获得成功的是( )
| A、将乙醛滴入银氨溶液中,加热煮沸制银镜 |
| B、苯与浓溴水反应制取溴苯 |
| C、CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型 |
| D、用CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热 |
向100ml 2mol/L的AlCl3溶液中加入未知浓度的NaOH溶液100ml,产生7.8g沉淀.则此NaOH溶液的物质的量浓度可能是( )
| A、2mol/L |
| B、1.5mol/L |
| C、3mol/L |
| D、7mol/L |