氢硫酸在空气中有如此反应:2H2S+O2═2S↓+2H2O,下列不正确的是( )
| A、属于置换反应 |
| B、还原性:H2O>H2S |
| C、氧化性:O2>S |
| D、酸性:H2S>H2O |
室温下将CH3COOH溶液与NaOH溶液等体积混合,结果混合液的pH=7,则CH3COOH溶液的物质的量浓度C1与NaOH溶液的C2的关系是( )
| A、C1=C2 |
| B、C1>C2 |
| C、C1<C2 |
| D、C1≥C2 |
下列的叙述中正确的是( )
| A、构成原电池的正极和负极的材料必须是两种活泼性不同的金属 |
| B、原电池是把化学能转变为电能的装置 |
| C、把铜片插入FeCl3溶液中,在铜片表面出现一层铁 |
| D、原电池工作时,正极和负极上发生的都是氧化还原反应 |
下列离子方程式与所述事实不相符的是( )
| A、苯酚钠溶液中通入少量CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- | ||
| B、在碳酸氢钠溶液中加入过量的氢氧化钡溶液:Ba2++OH-+HCO3-═BaCO3↓+H2O | ||
C、用新制的氢氧化铜悬浊液检验乙醛中的醛基:CH3CHO+2Cu(OH)2+OH-
| ||
| D、向Ca(ClO)2溶液中通入过量SO2:Ca2++2ClO-+SO2+H2O=CaSO4↓+2H++Cl-+HClO |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、能使甲基橙变黄的溶液中:Na+、K+、SO42-、AlO2- |
| B、水电离产生的c(H+)=1×10-12mol/L溶液:CH3COOH、Na+、Cl-、I- |
| C、能使pH试纸变深蓝色的溶液中:Na+、AlO2-、S2-、CO32- |
| D、0.1 mol?L-1NaHCO3溶液中:K+、Ba2+、OH-、Cl- |
下列关于氯水的叙述正确的是( )
| A、新制氯水可使蓝色石蕊试纸先变红后褪色 |
| B、新制氯水中只含Cl2和H2O分子 |
| C、光照氯水有气泡放出,该气体主要是Cl2 |
| D、氯水放置数天后酸性将减弱 |
下列化常用语中,正确的是( )
| A、两个氧分子-O2 |
| B、氢氧化铁的化学式-Fe(OH)3 |
| C、CO2中氧元素的化合价为+2价 |
| D、水通电得到氧气的化学方程式是2H2O=O2↑+2H2↑ |
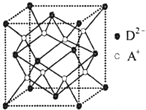 有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数.R是由A、D两元素形成的离子化合物,其中A+与D2-离子数之比为2:1.谙冋答下列问题:
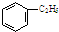
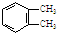
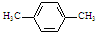
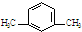
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数.R是由A、D两元素形成的离子化合物,其中A+与D2-离子数之比为2:1.谙冋答下列问题: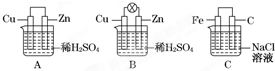 观察图A、B、C,回答下列问题:
观察图A、B、C,回答下列问题: