��Ŀ����
 �۲�ͼA��B��C���ش��������⣺
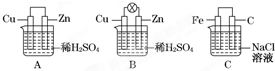
�۲�ͼA��B��C���ش��������⣺��1����һ�鴿����пƬ����װ��ϡ������ձ���ɹ۲쵽пƬ�������ݣ���ƽ�в���һ��ͭƬ���ɹ۲쵽ͭƬ
��2������ձ������װ�����2mol/L 500mL��ϡ������Һ������ͭпԭ��أ���ͼB���������������û����ʧ�������ڱ�״�����ռ���11.2L ������ʱ�����ʱ�ձ�����Һ�����ʵ����ʵ���Ũ�ȷֱ�Ϊ����Һ����仯���Բ��ƣ�
��3������缫���Ϸֱ�����Ƭ��ʯī���������ӣ������Ȼ�����Һ�У���ͼC���������������Ҫ����
��4������������ԭ���ԭ�������˸��ָ����ĵ�أ��ϵ�ر�����м��д����������ѱ��ᵽ�����ճ̣�������Ҫԭ����
A���������õ����ǵĽ���
B����ֹ����й����Ӻ�Ǧ���ؽ������Ӷ�������ˮԴ����Ⱦ
C����ֹ�������й�ĵ��Һ��ʴ������Ʒ
D���������е�ʯī�缫��
���㣺ԭ��غ͵��صĹ���ԭ��
ר�⣺�绯ѧר��
��������1������ͭ�������Ӧ��пƬ��ͭƬ�������γɵ�ԭ����У�����ͭΪ������пΪ������
��2�����ݵ缫��Ӧ����ʽ�����㣻
��3����Ƭ��ʯī���Ȼ�����Һ���ɵ�ԭ����У�����������������ʴ��
��4���Ͼɵ�غ����ؽ������ӣ�Ӧ��ֹ�ؽ�����Ⱦ��
��2�����ݵ缫��Ӧ����ʽ�����㣻
��3����Ƭ��ʯī���Ȼ�����Һ���ɵ�ԭ����У�����������������ʴ��
��4���Ͼɵ�غ����ؽ������ӣ�Ӧ��ֹ�ؽ�����Ⱦ��
���
�⣺��1��ϡ�����Zn�����û���Ӧ������������Cu����Ӧ������ͭƬ��û�����ݣ��õ��߰�пƬ��ͭƬ�������������һ��ԭ��أ�п��ʧ������������ͭ�������������������ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ2H++2e-=H2�����ʴ�Ϊ��û�У�п��2H++2e-=H2����
��2������������Ӧ��2H++2e-=H2�������ڱ�״�����ռ���11.2L��0.5mol������ʱ��ת�Ƶ�����1mol�����ٵ�������Ϊ1mol����������0.5mol����ʣ����������ʵ���Ϊ2mol/L��0.5L-0.5mol=0.5mol��
����ʣ��������Ũ��Ϊ1mol/L�������ϵĵ缫��ӦʽΪ��Zn��Zn2++2e-����ת�Ƶ���1molʱ������п���ӵ���Ϊ0.5mol������c��ZnSO4��=
=1mol/L��
�ʴ�Ϊ��c��H2SO4��=1mol/L��c��ZnSO4��=1mol/L��
��3����Ƭ��ʯī���Ȼ�����Һ���ɵ�ԭ����У�����������������ʴ���������������õ��ӷ������缫��ӦΪ��O2+2H2O+4e-=4OH-���ʴ�Ϊ��������O2+2H2O+4e-=4OH-��
��4���Ͼɵ���к��й����Ӻ�Ǧ���ؽ���Ԫ�أ��������к�����������ˮԴ����Ⱦ���������ⶪ������ʯī�缫��������ǵȻ��յļ�ֵ���Ǻܴ���Ҫ������Ⱦ���⣮
�ʴ�Ϊ��B��
��2������������Ӧ��2H++2e-=H2�������ڱ�״�����ռ���11.2L��0.5mol������ʱ��ת�Ƶ�����1mol�����ٵ�������Ϊ1mol����������0.5mol����ʣ����������ʵ���Ϊ2mol/L��0.5L-0.5mol=0.5mol��
����ʣ��������Ũ��Ϊ1mol/L�������ϵĵ缫��ӦʽΪ��Zn��Zn2++2e-����ת�Ƶ���1molʱ������п���ӵ���Ϊ0.5mol������c��ZnSO4��=
| 0.5mol |
| 0.5L |
�ʴ�Ϊ��c��H2SO4��=1mol/L��c��ZnSO4��=1mol/L��
��3����Ƭ��ʯī���Ȼ�����Һ���ɵ�ԭ����У�����������������ʴ���������������õ��ӷ������缫��ӦΪ��O2+2H2O+4e-=4OH-���ʴ�Ϊ��������O2+2H2O+4e-=4OH-��
��4���Ͼɵ���к��й����Ӻ�Ǧ���ؽ���Ԫ�أ��������к�����������ˮԴ����Ⱦ���������ⶪ������ʯī�缫��������ǵȻ��յļ�ֵ���Ǻܴ���Ҫ������Ⱦ���⣮
�ʴ�Ϊ��B��
���������⿼����̽��ԭ��ع����������缫��Ӧʽ����д��֪ʶ�㣬���ݼס����ж��ƶ�����������ͬʱ����ѧ���������⡢�ܽ������������Ŀ�ѶȲ���

��ϰ��ϵ�д�
 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�
�����Ŀ
�����£�0.1mol?L-1ijһԪ�ᣨHA����Һ��c��OH-��=1��10-11mol?L-1������������ȷ���ǣ�������
| A����һԪ����Һ��pH=1 | ||
| B������Һ��ˮ�����ӻ�����Ϊ1��10-22 | ||
| C������Һ��HA�ĵ����Ϊ 0.1% | ||
D������ˮϡ�ͣ���
|
������������ȷ���ǣ�������
| A��1mol���������1g |
| B��1molCO������Ϊ28g?mol-1 |
| C�������ӵ���������6.02��1023 |
| D��3.01��1023��SO2����Լ��0.5mol |
 ���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯����������������������Ҫ���ã���ش��������⣺
���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯����������������������Ҫ���ã���ش��������⣺