短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( ) 

| A、元素X与元素Z的最高正化合价之和的数值等于8 |
| B、元素Y、W的气态氢化物的稳定性,前者比后者差 |
| C、离子Y2-和Z3+的离子半径,后者比前者大 |
| D、元素W的最高价氧化物对应的水化物酸性比Q的强 |
工业上用含Fe2O3杂质的铝土矿为原料冶炼铝的工艺流程如下:下列叙述正确的是( )
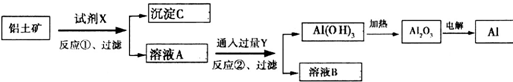

| A、反应①中试剂X是氢氧化钠溶液 |
| B、试剂Y是HCl,它与[Al(OH)4]-反应生成氢氧化铝 |
| C、图中所示转化反应中包含2个氧化还原反应 |
| D、将X与Y试剂进行对换,最终可以达到相同结果 |
下列实验操作或描述中,错误的是( )
| A、将等物质的量的NaNO3和KCl的混合液加热并浓缩至有晶体析出,趁热过滤时,可分离出NaCl晶体 |
| B、亚硝酸银和氯化银都是白色沉淀,故不能用硝酸银和稀硝酸溶液来区别亚硝酸钠与氯化钠 |
| C、冷却结晶时,如未出现结晶,可以用玻璃棒摩擦瓶壁并将锥形瓶置于冰水中冷却,促使晶体析出 |
| D、在适量氯化钴的乙醇溶液中,逐滴加入水至溶液恰好呈粉红色,加热该溶液,结果依次呈现紫色、蓝紫色、蓝色的变化 |
1mol某气态烃与5mol氧气在密闭容器中点燃,烃和氧气全部耗尽,测得生成4mol H2O(g)、2mol CO2和2mol CO(气体体积均在同温同压下测定)该烃的分子式是( )
| A、C4H10 |
| B、C3H8 |
| C、C4H8 |
| D、C2H4 |
下列对H2(g)+Cl2(g)═2HCl(g)△H(298K)=一184.6kJ?mol-1的叙述正确的是( )
| A、1分子H2和Cl2反应,放出热量184.6kJ |
| B、1mol H2 (g)完全反应生成2mol HCl(g),放出的热量为184.6kJ |
| C、在101 kPa、25℃的条件下,1mol H2(g)和1mol Cl2(g)完全反应生成2mol HCl(g)放出的热量为184.6kJ |
| D、在101 kPa、25℃的条件下,1mol H2和1mol Cl2完全反应生成2mol HCl(g)吸收的热量为184.6kJ |
下列有关有机化合物的组成、性质的说法,正确的( )
| A、天然气、液化石油气的成分相同 |
| B、葡萄糖、淀粉和乙酸乙酯在一定条件下都能发生水解反应 |
| C、淀粉、蛋白质均属于高分子化合物,而油脂不属于高分子化合物 |
| D、石油的裂解是化学变化,而石油的分馏和煤的干馏都是物理变化 |
逻辑推理是化学学习中常用的一种思维方法,以下推理中正确的是( )
| A、化合物都是由不同元素组成的,不同元素组成的物质一定是化合物 |
| B、金属镁排在金属活动性顺序表中氢元素的前面,所以其与稀硝酸反应一定放出氢气 |
| C、常温下,碱的水溶液的pH>7,则pH>7的水溶液一定是碱的水溶液 |
| D、氧化物中都含有氧元素,含氧元素的化合物不一定是氧化物 |
下列关于甘氨酸(H2N-CH2-COOH)性质的说法,正确的是( )
| A、只有酸性,没有碱性 |
| B、只有碱性,没有酸性 |
| C、既有酸性,又有碱性 |
| D、既没有酸性,又没有碱性 |
把100mL 2mol/L的H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应速率而不影响生成H2的总量,可在反应物中加入适量的( )
| A、硫酸铜溶液 |
| B、硝酸钠溶液 |
| C、醋酸钠溶液 |
| D、氢氧化钠溶液 |
下列说法正确的是( )
| A、因为SO2有漂白性,能使品红溶液永久褪色 |
| B、SO2具有还原性,能与强氧化性的高锰酸钾发生氧化还原反应 |
| C、大气中SO2浓度高时能形成酸雨,原因是SO2与雨水反应生成了H2SO3 |
| D、浓硫酸常用作干燥剂,是因为浓硫酸具有脱水性 |