工业炼铁是在高炉中进行的,高炉炼铁的主要反应是:①2C(焦炭)+O2(空气)=2CO;②Fe2O3+3CO=2Fe+3CO该炼铁工艺中,对焦炭的实际使用量要远远高于按照化学方程式计算所需其主要原因是:( )
| A、CO过量 |
| B、CO与铁矿石接触不充分 |
| C、炼铁高炉的高度不够 |
| D、CO与Fe2O3的反应有一定限度 |
下列物质中,能导电是( )
| A、氯化钠晶体 |
| B、澄清石灰水 |
| C、酒精 |
| D、CO2 |
下列化学用语使用正确的是( )
A、氟化镁的电子式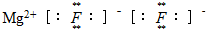 |
B、用电子式表示硫化氢的形成过程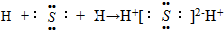 |
| C、HClO的结构式 H-O-Cl |
D、Cl-离子的结构示意图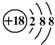 |
下列说法中,正确的是( )
| A、22.4L的HCl含有6.02×1023个粒子 |
| B、32g氧气中含有2mol的氧原子 |
| C、氢氧化钠的摩尔质量为40g |
| D、如果有6.02×1023颗大米,则这些大米的物质的量为1mol |
已知乙烯分子是平面结构,因此1,2-二氯乙烯可形成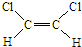 和
和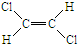 两种不同的空间异构体,称为顺反异构.下列能形成类似上述空间异构体的是( )
两种不同的空间异构体,称为顺反异构.下列能形成类似上述空间异构体的是( )
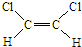 和
和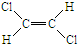 两种不同的空间异构体,称为顺反异构.下列能形成类似上述空间异构体的是( )
两种不同的空间异构体,称为顺反异构.下列能形成类似上述空间异构体的是( )| A、1-丁烯 | B、2-甲基-1-丙烯 |
| C、2-丁烯 | D、丁烷 |
下述实验能达到预期目的是( )
| 实验内容 | 实验目的 | |
| ① | 分别测定0.01mol/L的HCl和H2S的c(H+) | 比较氯和硫的非金属性强弱 |
| ② | 混合气体通入盛有饱和碳酸氢钠溶液的洗气瓶 | 除去CO2中少量的SO2 |
| ③ | 将SO2通入酸性KMnO4溶液中 | 证明SO2具有氧化性 |
| ④ | 将硫酸铜晶体分别放入浓硫酸和稀硫酸中 | 鉴别浓硫酸和稀硫酸 |
| A、②④ | B、①③ | C、①② | D、①④ |
 如图是物质A、B、C的溶解度曲线,下列相关说法正确的是( )
如图是物质A、B、C的溶解度曲线,下列相关说法正确的是( ) ①若要将B从溶液中结晶出来常采用的方法是蒸发结晶.
②将T2℃时A、B、C的饱和溶液冷却到T1℃,A溶液的质量分数最小.
③若要将组成在M点的A溶液转变为N点的溶液,只能采取恒温蒸发溶剂的方法.
④将T2℃时组成在M点的C 与水的混合物降温到T1℃,可得到C的不饱和溶液.
| A、①②③④ | B、①③④ |
| C、①④ | D、①②④ |
糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同.下列分析正确的是( )
| A、脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| B、含2.24g铁粉的脱氧剂,理论上最多能吸收氧气672mL(标准状况) |
| C、脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4 e-=4OH- |
| D、脱氧过程中铁作原电池正极,电极反应为:Fe-2e-=Fe2+ |