题目内容
糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同.下列分析正确的是( )
| A、脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| B、含2.24g铁粉的脱氧剂,理论上最多能吸收氧气672mL(标准状况) |
| C、脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4 e-=4OH- |
| D、脱氧过程中铁作原电池正极,电极反应为:Fe-2e-=Fe2+ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.脱氧过程为放热反应;
B.脱氧时,铁失去电子的物质的量=
×2=0.08mol,根据转移电子相等计算吸收氧气体积;
C.铁易失电子作负极、C作正极,正极上氧气得电子发生还原反应;
D.铁作负极、C作正极,负极上铁失电子发生氧化反应.
B.脱氧时,铁失去电子的物质的量=
| 2.24g |
| 56g/mol |
C.铁易失电子作负极、C作正极,正极上氧气得电子发生还原反应;
D.铁作负极、C作正极,负极上铁失电子发生氧化反应.
解答:
解:A.脱氧过程发生氧化还原反应,为放热反应,故A错误;
B.脱氧时,负极反应式为Fe-2e-=Fe2+,铁失去电子的物质的量=
×2=0.08mol,正极反应式为2H2O+O2+4e-=4OH-,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁被氧化生成氢氧化铁,
所以实际上铁元素转移电子物质的量=
×3=0.12mol,根据转移电子相等得吸收氧气体积=
×22.4L/mol=672mL,故B正确;
C.铁易失电子作负极、C作正极,正极上氧气得电子发生还原反应,电极反应式为2H2O+O2+4 e-=4OH-,故C错误;
D.铁作负极、C作正极,负极上铁失电子发生氧化反应,电极反应式为Fe-2e-=Fe2+,故D错误;
故选B.
B.脱氧时,负极反应式为Fe-2e-=Fe2+,铁失去电子的物质的量=
| 2.24g |
| 56g/mol |
所以实际上铁元素转移电子物质的量=
| 2.24g |
| 56g/mol |
| 0.12mol |
| 4 |
C.铁易失电子作负极、C作正极,正极上氧气得电子发生还原反应,电极反应式为2H2O+O2+4 e-=4OH-,故C错误;
D.铁作负极、C作正极,负极上铁失电子发生氧化反应,电极反应式为Fe-2e-=Fe2+,故D错误;
故选B.
点评:本题考查了原电池原理,明确整个过程中发生的反应是解本题关键,注意B中铁元素最终转化为氢氧化铁,为易错点.

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
下列图中的实验方案,能达到实验目的是( )
A、 验证FeCl3对H2O2分解反应有催化作用 |
B、 探究温度对平衡2NO2═N2O4的影响 |
C、 除去CO2气体中混有的HCl |
D、 比较HCl、H2CO3和H2SiO3的酸性强弱 |
下列说法中正确的是( )
| A、蔗糖和麦芽糖互为同分异构体 |
| B、乙酸乙酯和食用植物油均可水解生成乙醇 |
C、用甘氨酸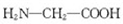 和丙氨酸 和丙氨酸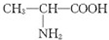 缩合最多可形成3种二肽 缩合最多可形成3种二肽 |
| D、合成聚乙烯塑料、酚醛塑料和聚苯乙烯塑料所发生的反应类型相同 |
无色难溶于水的气体是( )
| A、SO2 |
| B、NO |
| C、Cl2 |
| D、NO2 |
下列化学用语使用正确的是( )
A、氟化镁的电子式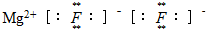 |
B、用电子式表示硫化氢的形成过程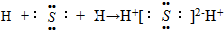 |
| C、HClO的结构式 H-O-Cl |
D、Cl-离子的结构示意图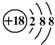 |
有机物分子中含有40个电子,它燃烧时生成等体积的CO2和H2O,该有机物的分子式为( )
| A、C4H8 |
| B、C4H10O |
| C、C5H10 |
| D、C4H10 |
下列说法正确的是( )
| A、在标准状况下,1摩尔任何物质的体积都约为22.4升 |
| B、22.4升氧气所含的氧原子数为2 NA个 |
| C、在标准状况下,1摩尔水的体积约为22.4升 |
| D、1摩尔某气体的体积约为22.4升时,该气体不一定处于标准状况下 |