0 133420 133428 133434 133438 133444 133446 133450 133456 133458 133464 133470 133474 133476 133480 133486 133488 133494 133498 133500 133504 133506 133510 133512 133514 133515 133516 133518 133519 133520 133522 133524 133528 133530 133534 133536 133540 133546 133548 133554 133558 133560 133564 133570 133576 133578 133584 133588 133590 133596 133600 133606 133614 203614

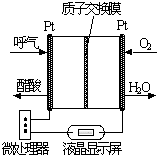
 微生物燃料电池(MFC)是燃料电池中特殊的一类,它利用微生物作为反应主体.将有机物的化学能转化为电能.以葡萄糖溶液作底物为例,其工作原理如图所示.
微生物燃料电池(MFC)是燃料电池中特殊的一类,它利用微生物作为反应主体.将有机物的化学能转化为电能.以葡萄糖溶液作底物为例,其工作原理如图所示.
 研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义.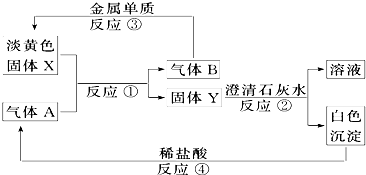
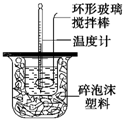 在量热器中将50ml、0.50mol?L-1CH3COOH溶液与50ml、0.55mol?L-1NaOH溶液混合,温度从25.16℃升高到27.46℃.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J?0C-1,C=4.18J?g-1?0C-1,溶液的密度为1g?cm-3.
在量热器中将50ml、0.50mol?L-1CH3COOH溶液与50ml、0.55mol?L-1NaOH溶液混合,温度从25.16℃升高到27.46℃.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J?0C-1,C=4.18J?g-1?0C-1,溶液的密度为1g?cm-3.