题目内容
Ⅰ、下列实验操作或对实验事实的描述正确的是 .
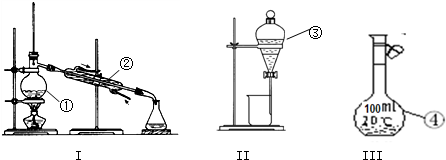
①用量筒量取稀硫酸溶液8.0mL;
②中和热的测定实验中,可用金属丝(棒)代替环形搅拌玻璃棒;
③用热的浓盐酸洗涤附着有MnO2的试管;
④在硫酸铜晶体结晶水含量的测定中,若加热后的无水硫酸铜粉末表面发黑,则所测结晶水含量可能会偏高;
⑤Fe(OH)3胶体与FeCl3溶液可用过滤的方法分离;
⑥用碱式滴定管量得KMnO4溶液20.50mL;
⑦将水沿烧杯内壁缓缓注入浓硫酸中,不断用玻璃棒搅拌以稀释浓硫酸;
⑧用湿润的pH试纸测量某溶液pH时,测量值一定比真实值小;
⑨锌和一定量稀硫酸反应,为加快速率而不影响H2的量可向溶液中加适量Cu(NO3)2晶体.
Ⅱ、2013年初,雾霾天气多次肆虐天津、北京等地区.其中,燃煤和汽车尾气是造成空气污染的原因之一.

(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)
2CO2(g)+N2(g)△H<0
①该反应平衡常数表达式 .
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号).
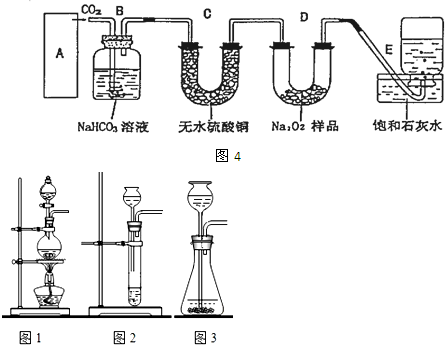
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.
煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOX可以消除氮氧化物的污染.已知:
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ/mol
2NO2(g)?N2O4(g)△H=-56.9kJ/mol
H2O(g)=H2O(l)△H=-44.0kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式: .
①用量筒量取稀硫酸溶液8.0mL;
②中和热的测定实验中,可用金属丝(棒)代替环形搅拌玻璃棒;
③用热的浓盐酸洗涤附着有MnO2的试管;
④在硫酸铜晶体结晶水含量的测定中,若加热后的无水硫酸铜粉末表面发黑,则所测结晶水含量可能会偏高;
⑤Fe(OH)3胶体与FeCl3溶液可用过滤的方法分离;
⑥用碱式滴定管量得KMnO4溶液20.50mL;
⑦将水沿烧杯内壁缓缓注入浓硫酸中,不断用玻璃棒搅拌以稀释浓硫酸;
⑧用湿润的pH试纸测量某溶液pH时,测量值一定比真实值小;
⑨锌和一定量稀硫酸反应,为加快速率而不影响H2的量可向溶液中加适量Cu(NO3)2晶体.
Ⅱ、2013年初,雾霾天气多次肆虐天津、北京等地区.其中,燃煤和汽车尾气是造成空气污染的原因之一.

(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)
| 催化剂 |
①该反应平衡常数表达式
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.
煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOX可以消除氮氧化物的污染.已知:
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ/mol
2NO2(g)?N2O4(g)△H=-56.9kJ/mol
H2O(g)=H2O(l)△H=-44.0kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:
考点:化学实验方案的评价,热化学方程式,化学平衡建立的过程,化学平衡状态的判断
专题:实验评价题,化学平衡专题
分析:Ⅰ、①量筒感量是0.1mL;
②中和热的测定实验中,不能用金属丝(棒)代替环形搅拌玻璃棒;
③加热条件下,浓盐酸和二氧化锰反应生成可溶性氯化锰;
④在硫酸铜晶体结晶水含量的测定中,若加热后的无水硫酸铜粉末表面发黑,导致部分硫酸铜分解;
⑤Fe(OH)3胶体与FeCl3溶液都能透过滤纸;
⑥碱式滴定管只能盛放碱溶液;
⑦稀释浓硫酸时,浓硫酸倒入水中;
⑧用湿润的pH试纸测量某溶液pH时,导致所测溶液浓度偏低;
⑨锌和硝酸反应生成NO.
Ⅱ、(1)①平衡常数等于生成物浓度的幂之积比上反应浓度幂之积;
②a、到达平衡后正、逆速率相等,不再变化;
b、到达平衡后,温度为定值,平衡常数不变,结合反应热判断随反应进行容器内温度变化,判断温度对化学平衡常数的影响;
c、t1时刻后二氧化碳、CO的物质的量发生变化,最后不再变化;
d、到达平衡后各组分的含量不发生变化;
(2)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减构造目标热化学方程式.
②中和热的测定实验中,不能用金属丝(棒)代替环形搅拌玻璃棒;
③加热条件下,浓盐酸和二氧化锰反应生成可溶性氯化锰;
④在硫酸铜晶体结晶水含量的测定中,若加热后的无水硫酸铜粉末表面发黑,导致部分硫酸铜分解;
⑤Fe(OH)3胶体与FeCl3溶液都能透过滤纸;
⑥碱式滴定管只能盛放碱溶液;
⑦稀释浓硫酸时,浓硫酸倒入水中;
⑧用湿润的pH试纸测量某溶液pH时,导致所测溶液浓度偏低;
⑨锌和硝酸反应生成NO.
Ⅱ、(1)①平衡常数等于生成物浓度的幂之积比上反应浓度幂之积;
②a、到达平衡后正、逆速率相等,不再变化;
b、到达平衡后,温度为定值,平衡常数不变,结合反应热判断随反应进行容器内温度变化,判断温度对化学平衡常数的影响;
c、t1时刻后二氧化碳、CO的物质的量发生变化,最后不再变化;
d、到达平衡后各组分的含量不发生变化;
(2)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减构造目标热化学方程式.
解答:
解:Ⅰ、①量筒感量是0.1mL,所以可以用量筒量取稀硫酸溶液8.0mL,故正确;
②中和热的测定实验中,不能用金属丝(棒)代替环形搅拌玻璃棒,因为金属棒会传递热量,导致测量结果偏小,故错误;
③热的浓盐酸和二氧化锰反应生成可溶性氯化锰,稀盐酸和二氧化锰不反应,故正确;
④在硫酸铜晶体结晶水含量的测定中,若加热后的无水硫酸铜粉末表面发黑,导致部分硫酸铜分解,固体减少的质量增大,则所测结晶水含量可能会偏高,故正确;
⑤Fe(OH)3胶体与FeCl3溶液都能透过滤纸,所以不能用过滤的方法分离,应该用渗析的方法分离,故错误;
⑥高锰酸钾溶液呈酸性,只能用酸式滴定管量取,故错误;
⑦将浓硫酸沿烧杯内壁缓缓注入水中,为防止局部温度过高而溅出液体,不断用玻璃棒搅拌以稀释浓硫酸,故错误;
⑧用湿润的pH试纸测量某溶液pH时,溶液浓度偏小,导致测量不准确,故错误;
⑨锌和硝酸铜的酸性溶液反应生成NO,从而影响生成氢气的量,故错误;
故选①③④;
Ⅱ、(1)①平衡常数等于生成物浓度的幂之积比上反应浓度幂之积,即:K=
,故答案为:K=
;
②a、到达平衡后正、逆速率相等,不再变化,t1时刻V正最大,之后随反应进行速率发生变化,未到达平衡,故a错误;
b、该反应正反应为放热反应,随反应进行温度升高,化学平衡常数减小,到达平衡后,温度为定值,达最高,平衡常数不变,为最小,图象与实际符合,故b正确;
c、t1时刻后二氧化碳、CO的物质的量发生变化,t1时刻未到达平衡状态,故c错误;
d、NO的质量分数为定值,t1时刻处于平衡状态,故d正确,
故答案为:bd;
(2)已知:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H1=-867kJ/mol①
2NO2(g)?N2O4(g)△H2=-56.9kJ/mol②
H2O(g)=H2O(l)△H=-44.0kJ/mol③
根据盖斯定律,①-②+④×2可得CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g),故△H=-867kJ/mol-(-56.9kJ/mol)+2(-44.0)kJ/mol=-898.1kJ/mol 即CH4(g)+N2O4(g)═N2(g)+2H2O(g)+CO2(g)△H=-898.1kJ/mol,
故答案为:CH4(g)+N2O4(g)═N2(g)+2H2O(g)+CO2(g)△H=-898.1kJ/mol.
②中和热的测定实验中,不能用金属丝(棒)代替环形搅拌玻璃棒,因为金属棒会传递热量,导致测量结果偏小,故错误;
③热的浓盐酸和二氧化锰反应生成可溶性氯化锰,稀盐酸和二氧化锰不反应,故正确;
④在硫酸铜晶体结晶水含量的测定中,若加热后的无水硫酸铜粉末表面发黑,导致部分硫酸铜分解,固体减少的质量增大,则所测结晶水含量可能会偏高,故正确;
⑤Fe(OH)3胶体与FeCl3溶液都能透过滤纸,所以不能用过滤的方法分离,应该用渗析的方法分离,故错误;
⑥高锰酸钾溶液呈酸性,只能用酸式滴定管量取,故错误;
⑦将浓硫酸沿烧杯内壁缓缓注入水中,为防止局部温度过高而溅出液体,不断用玻璃棒搅拌以稀释浓硫酸,故错误;
⑧用湿润的pH试纸测量某溶液pH时,溶液浓度偏小,导致测量不准确,故错误;
⑨锌和硝酸铜的酸性溶液反应生成NO,从而影响生成氢气的量,故错误;
故选①③④;
Ⅱ、(1)①平衡常数等于生成物浓度的幂之积比上反应浓度幂之积,即:K=
| C(N2)C2(CO2) |
| C2(NO)C2(CO) |
| C(N2)C2(CO2) |
| C2(NO)C2(CO) |
②a、到达平衡后正、逆速率相等,不再变化,t1时刻V正最大,之后随反应进行速率发生变化,未到达平衡,故a错误;
b、该反应正反应为放热反应,随反应进行温度升高,化学平衡常数减小,到达平衡后,温度为定值,达最高,平衡常数不变,为最小,图象与实际符合,故b正确;
c、t1时刻后二氧化碳、CO的物质的量发生变化,t1时刻未到达平衡状态,故c错误;
d、NO的质量分数为定值,t1时刻处于平衡状态,故d正确,
故答案为:bd;
(2)已知:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H1=-867kJ/mol①
2NO2(g)?N2O4(g)△H2=-56.9kJ/mol②
H2O(g)=H2O(l)△H=-44.0kJ/mol③
根据盖斯定律,①-②+④×2可得CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g),故△H=-867kJ/mol-(-56.9kJ/mol)+2(-44.0)kJ/mol=-898.1kJ/mol 即CH4(g)+N2O4(g)═N2(g)+2H2O(g)+CO2(g)△H=-898.1kJ/mol,
故答案为:CH4(g)+N2O4(g)═N2(g)+2H2O(g)+CO2(g)△H=-898.1kJ/mol.
点评:本题考查了实验方案评价,涉及盖斯定律求焓变、化学平衡影响因素,化学反应速率,平衡常数概念计算应用等知识点,明确实验原理是解本题关键,注意⑨中隐含条件,为易错点.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
甲、乙、丙均为中学化学常见的不同物质,它们的转化关系如图所示.甲不可能是( )


| A、NH4Cl |
| B、Al2O3 |
| C、SiO2 |
| D、CO2 |
下列说法正确的是( )
| A、海水中提取镁的过程中有用到硫酸 |
| B、工业炼铁中加入石灰石的目的是除去铁矿石中的杂质 |
| C、铁、铝常温下不能和浓硫酸、浓硝酸反应 |
| D、铝热反应特指铝与氧化铁的反应 |
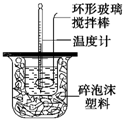 在量热器中将50ml、0.50mol?L-1CH3COOH溶液与50ml、0.55mol?L-1NaOH溶液混合,温度从25.16℃升高到27.46℃.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J?0C-1,C=4.18J?g-1?0C-1,溶液的密度为1g?cm-3.
在量热器中将50ml、0.50mol?L-1CH3COOH溶液与50ml、0.55mol?L-1NaOH溶液混合,温度从25.16℃升高到27.46℃.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J?0C-1,C=4.18J?g-1?0C-1,溶液的密度为1g?cm-3.