氢化钙可作为生氢剂,化学方程式是CaH2+2H2O═Ca(OH)2+2H2↑,下列有关叙述正确的是( )
| A、氢化钙被还原 |
| B、水既是氧化剂,又是还原剂 |
| C、H2既是氧化产物,也是还原产物 |
| D、H2O发生氧化反应 |
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1),下列说法错误的是( )
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的平衡浓度(mol?L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | a1 | a2 | a3 |
| A、2c1<c3 |
| B、a+b=92.4 |
| C、p3>2p2=2p1 |
| D、a1+a3<1 |
下列说法正确的是( )
| A、某微粒空间构型为直线形,则该微粒一定是非极性分子 |
| B、某微粒空间构型为V形,则中心原子一定是sp3杂化 |
| C、某微粒空间构型为平面三角形,则中心原子一定是sp2杂化 |
| D、某微粒空间构型为正四面体,则键角一定是109°28’ |
下列实验操作中正确的是( )
| A、蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B、蒸馏时,温度计水银球靠近蒸馏烧瓶的底部,且冷却水从冷凝管的下口通入上口流出 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、称量时,将Na2CO3固体直接放在托盘天平的右盘上 |
下列说法中正确的是( )
| A、需要加热才能发生的反应一定是吸热反应 |
| B、任何放热的反应在常温条件下一定能发生反应 |
| C、吸热反应只能在加热的条件下才能进行 |
| D、反应是放热还是吸热是由反应物和生成物所具有的总能量所决定的 |
下列叙述不正确的是( )
| A、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B、铜锌原电池工作时,电流沿外电路从铜电极流向锌电极 |
| C、把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 |
| D、为加快锌粒与盐酸反应的速率,可以向溶液中加入几滴氯化铜溶液 |
一定温度下,向一固定容积的容器中放入1mol A和1mol B,待反应A(s)+B(g)?C(g)+2D(g)达到平衡时,C的体积分数是M%,在相同的条件下,若按以下配比开始反应,平衡时C的体积分数比为M%的是( )
| A、2molA+2molB |
| B、1molD+2molC |
| C、2molD+1molA+1molB |
| D、1molA+0.5molB+0.5molC+1.0molD |
向含Al2(SO4)3和AlCl3的混合溶液中逐滴加入1mol/L Ba(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所得沉淀的物质的量的关系如图,下列说法不正确的是( )
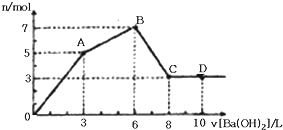

| A、OA段反应的离子方程式为:3Ba2++2Al3++8OH-+3SO42-═3BaSO4↓+2AlO2-+4H2O |
| B、向D点溶液中通入C02气体,立即产生白色沉淀 |
| C、原混合液中c[Al2(SO4)3]:c(AlCl3)═1:2 |
| D、图中C点铝元素存在形式是AlO2- |
向某密闭容器中充入1mol CO和2mol H2O(g),发生反应:CO+H2O(g)
CO2+H2.当反应达到平衡时,CO2的浓度为xmol/L.若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO2的体积仍为xmol/L的是( )
| 催化剂 |
| 高温 |
| A、0.5 mol CO+1 mol H2O(g) |
| B、1 mol CO+1 mol CO2+1 mol H2 |
| C、1 mol CO2+1 mol H2 |
| D、2mol CO+4 mol H2O(g) |
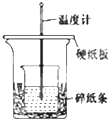 某实验小组学生用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如
某实验小组学生用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中进行试验测定中和热.下列说法正确的是( )
| A、烧杯间填满碎纸条的作用是固定小烧杯 |
| B、图中装置还需要增加一根玻璃棒进行搅拌 |
| C、量取NaOH溶液的体积时仰视进行操作,会使测出的中和热数值偏高 |
| D、若改用60 mL 0.55 mol/L盐酸与40 mL 0.50 mol/L的NaOH溶液进行反应,从理论上讲测出的中和热不变 |