题目内容
向某密闭容器中充入1mol CO和2mol H2O(g),发生反应:CO+H2O(g)
CO2+H2.当反应达到平衡时,CO2的浓度为xmol/L.若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO2的体积仍为xmol/L的是( )
| 催化剂 |
| 高温 |
| A、0.5 mol CO+1 mol H2O(g) |
| B、1 mol CO+1 mol CO2+1 mol H2 |
| C、1 mol CO2+1 mol H2 |
| D、2mol CO+4 mol H2O(g) |
考点:等效平衡
专题:化学平衡专题
分析:根据等效平衡解答,恒温恒容下,该反应前后气体体积不发生变化,平衡时CO2的浓度为xmol/L,则将物质全部转化到左边,要满足n(CO)=1mol,n(H2O)=2mol,或者1mol CO和2mol H2O(g)可以看作是在1mol CO和1mol H2O(g)的基础上再加1mol H2O(g),然后达到平衡,这与1mol CO和1mol H2O(g)的基础上再加1mol CO,达到平衡时CO2的浓度是一样的,也为xmol/L,据此解答.
解答:
解:根据等效平衡解答,恒温恒容下,该反应前后气体体积不发生变化,平衡时CO2的浓度为xmol/L,则将物质全部转化到左边,要满足n(CO)=1mol,n(H2O)=2mol,为完全等效平衡,
A.0.5 mol CO+1 mol H2O(g),不满足n(CO)=1mol,n(H2O)=2mol,故A错误;
B.1mol CO和2mol H2O(g)可以看作是在1mol CO和1mol H2O(g)的基础上再加1mol H2O(g),然后达到平衡,这与1mol CO和1mol H2O(g)的基础上再加1mol CO,达到平衡时CO2的浓度是一样的,也为xmol/L,故B正确;
C.1 mol CO2+1 mol H2,不满足n(CO)=1mol,n(H2O)=2mol,CO2的浓度小于xmol/L.故C错误;
D.2mol CO+4 mol H2O是1mol CO和2mol H2O(g)的两倍,所以平衡时CO2的浓度大于xmol/L,故D错误;
故选:B.
A.0.5 mol CO+1 mol H2O(g),不满足n(CO)=1mol,n(H2O)=2mol,故A错误;
B.1mol CO和2mol H2O(g)可以看作是在1mol CO和1mol H2O(g)的基础上再加1mol H2O(g),然后达到平衡,这与1mol CO和1mol H2O(g)的基础上再加1mol CO,达到平衡时CO2的浓度是一样的,也为xmol/L,故B正确;
C.1 mol CO2+1 mol H2,不满足n(CO)=1mol,n(H2O)=2mol,CO2的浓度小于xmol/L.故C错误;
D.2mol CO+4 mol H2O是1mol CO和2mol H2O(g)的两倍,所以平衡时CO2的浓度大于xmol/L,故D错误;
故选:B.
点评:本题考查了化学平衡的影响因素、等效平衡等,理解等效平衡规律是关键,题目难度中等.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
下列各图均能表示甲烷的分子结构,哪一种更能反映其真实存在状况( )
A、 甲烷分子结构示意 |
B、 甲烷分子的电子 |
C、 球棍模型 |
D、 比例模型 |
下列除去杂质的方法正确的是( )
| A、除去乙烷中少量的乙烯:通过酸性KMnO4溶液进行分离 |
| B、除去溴苯中少量的溴,可用苯进行洗涤、分液 |
| C、除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液,然后干燥、蒸馏 |
| D、除去氯气中少量的氯化氢,通过NaOH溶液进行分离 |
下列实验操作中正确的是( )
| A、蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B、蒸馏时,温度计水银球靠近蒸馏烧瓶的底部,且冷却水从冷凝管的下口通入上口流出 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、称量时,将Na2CO3固体直接放在托盘天平的右盘上 |
 如图所示的装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色.下列说法中正确的是( )
如图所示的装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色.下列说法中正确的是( )| A、X是负极,Y是正极 |
| B、Pt是阴极,Cu是阳极 |
| C、CuSO4溶液的酸性逐渐增强 |
| D、CuSO4溶液的酸性不变 |
海水中含有MgCl2,从海水中提取镁,正确的方法是( )
A、海水
| ||||||
B、海水
| ||||||
C、海水
| ||||||
D、海水
|
在一固定体积的密闭容器中,加入2mol A和1mol B发生反应2A(g)+B(g)?3C(g)+D(s),达到平衡,c的浓度为w mol/L.若维持容器体积和温度不变,下列四种配比作为起始物质,达平衡后,C的浓度仍为w mol/L的是 ( )
| A、4mol A+2mol B |
| B、2mol A+1mol B+1.5mol C+0.5mol |
| C、3mol C+1mol D+1mol B |
| D、3mol C+2mol D |
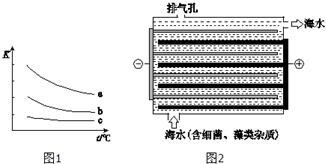 海水是巨大的化学资源宝库.
海水是巨大的化学资源宝库.