下列事实能说明醋酸属于弱电解质的是( )
①中和100ml,1mol/L CH3COOH溶液需要100ml,1mol/L NaOH溶液
②物质的量浓度相同的盐酸和醋酸同时与锌反应,开始时锌粒跟盐酸反应的速率比跟醋酸反应的速率快
③0.01mol/L醋酸溶液的pH=3
④将pH=2的醋酸溶液稀释1000倍后,2<pH<5.
①中和100ml,1mol/L CH3COOH溶液需要100ml,1mol/L NaOH溶液
②物质的量浓度相同的盐酸和醋酸同时与锌反应,开始时锌粒跟盐酸反应的速率比跟醋酸反应的速率快
③0.01mol/L醋酸溶液的pH=3
④将pH=2的醋酸溶液稀释1000倍后,2<pH<5.
| A、①②③ | B、②③④ |
| C、①③④ | D、①④ |
下列水溶液中的各组离子因为发生氧化还原反应而不能大量共存的是( )
| A、Na+、Ba2+、Cl-、SO42- |
| B、Ca2+、HCO3-、C1-、K+ |
| C、Fe3+、K+、I-、H+ |
| D、H+、Cl-、Na+、CO32- |
实验室中配制250mL 0.10mo1?L-1 NaOH溶液时,必须使用到的玻璃仪器是( )
A、 锥形瓶 |
B、 试管 |
C、 分液漏斗 |
D、 容量瓶 |
下列对酯化反应理解不正确的是( )
| A、酯化反应是有限度的 |
| B、酯化反应可以看成是取代反应的一种 |
| C、酯化反应的产物只有酯 |
| D、浓硫酸可作酯化反应的催化剂 |
下列每组均有四种物质,按照某种分类标准,其中有一种物质与其他三种物质的类别不同,每组中选出的该物质能够化合生成一种盐类化合物.该化合物的化学式为( )
①O2、Cl2、NO2、Br2
②铜、硅、硫、钠;
③CH4、NH3、H2O、HCl;
④CuO、Fe2O3、CO2、Na2O.
①O2、Cl2、NO2、Br2
②铜、硅、硫、钠;
③CH4、NH3、H2O、HCl;
④CuO、Fe2O3、CO2、Na2O.
| A、NH4HCO3 |
| B、Na2SiO3?2H2O |
| C、Cu2 (OH) 2CO3 |
| D、FeSO4?7H2O |
下列烷烃的系统命名正确的是( )
| A、2-乙基丁烷 |
| B、3,3-二甲基丁烷 |
| C、2-甲基-4-乙基庚烷 |
| D、3-乙基-2,3-二甲基戊烷 |
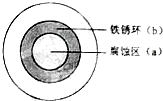 将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示.导致现象的主要原因是液滴之下氧气含量比边缘处少.下列说法正确的是( )
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示.导致现象的主要原因是液滴之下氧气含量比边缘处少.下列说法正确的是( )| A、液滴中的Cl - 由a区向b区迁移 |
| B、铁腐蚀严重的区域,生锈也严重 |
| C、液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH- 形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
| D、液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e-=4OH- |
对石油化学工业的叙述中正确的是( )
| A、分馏汽油和裂化汽油中加入溴的四氯化碳溶液均能发生反应 |
| B、催化裂化既能提高汽油的产量又能提高汽油的质量 |
| C、石油裂解的目的是提高汽油的产量 |
| D、石油减压分馏的目的是获得轻质油 |
有关溶液中离子的检验下列说法正确的是( )
| A、加入硝酸酸化,再滴加KSCN溶液后有红色物质生成,则原溶液中一定有Fe3+ |
| B、加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定有CO32- |
| C、先用盐酸酸化,再加入Ba(NO3)2溶液,有白色沉淀,则原溶液中一定有SO42- |
| D、分别含有MgCl2、FeCl3、CuCl2和NaCl的四种溶液,只用NaOH就可以一次鉴别开 |
下列叙述正确的是( )
| A、P4是非极性分子,磷原子处在正方形4个角上 |
| B、H2O是极性分子,氧原子不处在2个氢原子所连成的直线的中央 |
| C、CCl4是非极性分子,碳原子处在4个氯原子所组成的正方形的中心 |
| D、CO2是极性分子,碳原子处在2个氧原子所连成的直线的中央 |
| E、CO2是极性分子,碳原子处在2个氧原子所连成的直线的中央 |