题目内容
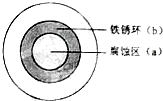 将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示.导致现象的主要原因是液滴之下氧气含量比边缘处少.下列说法正确的是( )
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示.导致现象的主要原因是液滴之下氧气含量比边缘处少.下列说法正确的是( )| A、液滴中的Cl - 由a区向b区迁移 |
| B、铁腐蚀严重的区域,生锈也严重 |
| C、液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH- 形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
| D、液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e-=4OH- |
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:铁板在氯化钠溶液中发生吸氧腐蚀,属于原电池,a作原电池负极、b作原电池正极,
A.放电时,阴离子向负极移动;
B.铁被腐蚀在负极上发生反应,生锈在正极上反应;
C.液滴下的铁发生氧化反应而被腐蚀;
D.液滴边缘是正极区,正极上氧气得电子发生还原反应.
A.放电时,阴离子向负极移动;
B.铁被腐蚀在负极上发生反应,生锈在正极上反应;
C.液滴下的铁发生氧化反应而被腐蚀;
D.液滴边缘是正极区,正极上氧气得电子发生还原反应.
解答:
解:铁板在氯化钠溶液中发生吸氧腐蚀,属于原电池,a作原电池负极、b作原电池正极,
A.放电时,Cl - 由b区向a区迁移,故A错误;
B.铁被腐蚀在负极上发生反应,生锈在正极上反应,所以铁腐蚀严重的区域,生锈不严重,故B错误;
C.液滴下的铁为负极,失电子发生氧化反应而被腐蚀,故C错误;
D.液滴边缘是正极区,正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-=4OH-,故D正确;
故选D.
A.放电时,Cl - 由b区向a区迁移,故A错误;
B.铁被腐蚀在负极上发生反应,生锈在正极上反应,所以铁腐蚀严重的区域,生锈不严重,故B错误;
C.液滴下的铁为负极,失电子发生氧化反应而被腐蚀,故C错误;
D.液滴边缘是正极区,正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-=4OH-,故D正确;
故选D.
点评:本题考查金属的吸氧腐蚀,明确各个电极上发生的反应及离子移动方向即可解答,会正确书写电极反应式,知道铁锈的成分,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、IA族元素的金属性一定比ⅡA族元素的金属性强 |
| B、ⅥA族中氢化物最稳定的元素,其最高价含氧酸的酸性也最强 |
| C、某一元素可能既显金属性,又显非金属性 |
| D、短周期中,同周期元素所形成的简单离子的半径,从左到右逐渐减小 |
下列水溶液中的各组离子因为发生氧化还原反应而不能大量共存的是( )
| A、Na+、Ba2+、Cl-、SO42- |
| B、Ca2+、HCO3-、C1-、K+ |
| C、Fe3+、K+、I-、H+ |
| D、H+、Cl-、Na+、CO32- |
下列说法不正确的是( )
| A、煤、石油、天然气均属于可再生的化石燃料 |
| B、糖类、油脂、蛋白质是人类重要的营养物质 |
| C、高温结构陶瓷、光导纤维均属于新型无机非金属材料 |
| D、塑料、合成纤维、合成橡胶是我们生活中常见的合成材料 |
用下列装置进行相应实验,能达到实验目的是( )
A、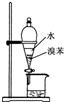 用如图所示装置分离出溴苯 |
B、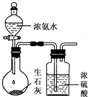 用如图所示装置制取干燥的氨气 |
C、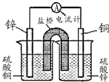 用如图设计成铜锌原电池装置 |
D、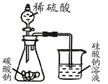 用如图证明氢化物稳定性SiH4>CH4>H2S |
苹果醋是一种由苹果发酵而成的食品.苹果酸(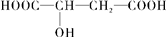 )是这种饮料的主要酸性物质.下列有关苹果酸性质的说法中,不正确的是( )
)是这种饮料的主要酸性物质.下列有关苹果酸性质的说法中,不正确的是( )
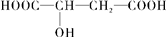 )是这种饮料的主要酸性物质.下列有关苹果酸性质的说法中,不正确的是( )
)是这种饮料的主要酸性物质.下列有关苹果酸性质的说法中,不正确的是( )| A、可以与NaHCO3溶液反应产生CO2 |
| B、可以与乙醇发生酯化反应 |
| C、1mol的苹果酸最多能与2mol金属钠反应 |
D、苹果酸与 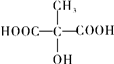 互为同分异构体 互为同分异构体 |