下列反应是吸热反应又是氧化还原反应的是( )
| A、镁与醋酸 |
| B、氯化铵与氢氧化钡晶体 |
| C、制水煤气的反应 |
| D、盐酸与氢氧化钠 |
过氧乙酸(CH3COOOH)是一种高效消毒剂,可以迅速杀灭多种微生物,包括多种病毒(如 SARS病毒)、细菌、真菌及芽孢.过氧乙酸可由冰醋酸与过氧化氢在一定条件下作用制得,有关过氧乙酸的叙述中正确的是( )
| A、过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体 | ||
| B、因含有过氧基“-O-O-”而有强氧化性 | ||
C、由下列过氧乙酸的制取原理可以看出,过氧乙酸是酯的同系物CH3COOH+H2O2
| ||
| D、过氧乙酸易分解生成乙酸和氧气,不可直接用手接触原液,使用时不可稀释 |
奥运五环代表着全世界五大洲的人民团结在一起.下列各项中的物质能满足如图中阴影部分关系的是( )


| A、①NaCl;②K2SO4;③KCl;④(NH4)2SO4; |
| B、①Na2SO4;②K2SO4;③KCl;④(NH4)2SO4; |
| C、①NaCl;②K2SO4;③KCl;④NH4Cl; |
| D、①Na2SO4;②K2SO4;③KCl;④NH4Cl. |
下列电离方程式中,正确的是( )
| A、Na2SO4═2Na++SO4-2 |
| B、Al(NO3)3═Al3++3NO3- |
| C、Ba(OH)2═Ba2++(OH-)2 |
| D、CuSO4═Cu2++S6++4O2- |
下列说法正确的是( )
| A、放热的反应在常温下一定易进行 |
| B、吸热反应在常温下不能进行 |
| C、有吸热或放热现象的过程中一定发生了化学反应 |
| D、反应是放热还是吸热是由反应物和生成物所具有的能量的相对大小决定的 |
用NA表示阿伏德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4LH2O含有的分子数为1NA |
| B、常温常压下,106gNa2CO3含有的Na+离子数为2NA |
| C、通常状况下,1NA个CO2分子占有的体积为22.4L |
| D、物质的量浓度为0.5mol?/L的MgCl2溶液中,含有Cl-个数为1NA |
能说明醋酸是弱电解质的事实是( )
| A、醋酸溶液的导电性比盐酸弱 |
| B、醋酸溶液与碳酸钙反应,缓慢放出二氧化碳 |
| C、0.1mol L-1的CH3COOH溶液中氢离子浓度约为0.001 mol L-1 |
| D、醋酸溶液用水稀释后,氢离子浓度下降 |
正确掌握好化学用语是学好化学的基础,下列有关表述正确物是( )
| A、乙烯的结构简式:CH2CH2 |
B、NH3的电子式: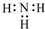 |
| C、NaHCO3水解的离子方程式:HCO3-+H2O?H3O++CO32- |
| D、亚硫酸氢根离子的电离方程式:HSO3-+H2O?H3O++SO32- |
下列各组仪器,常用于物质分离的是( )
①漏斗 ②容量瓶 ③温度计 ④分液漏斗 ⑤天平⑥量筒 ⑦胶头滴管 ⑧蒸馏烧瓶 ⑨集气瓶.
①漏斗 ②容量瓶 ③温度计 ④分液漏斗 ⑤天平⑥量筒 ⑦胶头滴管 ⑧蒸馏烧瓶 ⑨集气瓶.
| A、①④⑧ | B、②⑥⑦⑨ |
| C、①③⑦ | D、④⑤⑥⑧ |
室温时,已知Kb(NH3?H2O)═Ka(CH3COOH).关于浓度均为0.1mol/L的六种溶液:①氨水、②盐酸、③氯化铵、④硫酸氢铵、⑤醋酸钠、⑥氢氧化钠溶液,下列说法正确的是( )
| A、c(NH4+):①>④>③ |
| B、水电离出的c(H+):⑤>④>①>② |
| C、①和②等体积混合后的溶液:c(OH-)=c(H+)+c(NH3?H2O) |
| D、①和③等体积混合后的溶液:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |