题目内容
室温时,已知Kb(NH3?H2O)═Ka(CH3COOH).关于浓度均为0.1mol/L的六种溶液:①氨水、②盐酸、③氯化铵、④硫酸氢铵、⑤醋酸钠、⑥氢氧化钠溶液,下列说法正确的是( )
| A、c(NH4+):①>④>③ |
| B、水电离出的c(H+):⑤>④>①>② |
| C、①和②等体积混合后的溶液:c(OH-)=c(H+)+c(NH3?H2O) |
| D、①和③等体积混合后的溶液:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
考点:弱电解质在水溶液中的电离平衡,盐类水解的应用
专题:盐类的水解专题
分析:A、氨水是弱碱,能部分电离出铵根离子,氯化铵能电离出铵根离子,硫酸氢铵是盐溶液,能完全电离出氢离子、铵根离子和硫酸根离子,根据铵根离子的水解程度来回答;
B、酸和碱对水的电离起抑制作用,能水解的盐对水的电离起促进作用;
C、0.1mol/L的①氨水②盐酸等体积混合后生成氯化铵溶液,溶液中存在质子守恒,据此回答;
D、氨水和氯化铵的混合液显示碱性,据此确定溶液中离子浓度的关系.
B、酸和碱对水的电离起抑制作用,能水解的盐对水的电离起促进作用;
C、0.1mol/L的①氨水②盐酸等体积混合后生成氯化铵溶液,溶液中存在质子守恒,据此回答;
D、氨水和氯化铵的混合液显示碱性,据此确定溶液中离子浓度的关系.
解答:
解:A、氨水是弱碱,能部分电离出铵根离子,氯化铵、硫酸氢铵是盐溶液能完全电离出氢离子,硫酸氢铵中氢离子对铵根离子的水解起到抑制作用,所以c(NH4+):④>③>①,故A错误;
B、酸和碱对水的电离起抑制作用,盐酸的抑制作用大于氨水的抑制作用,能水解的盐对水的电离起促进作用,硫酸氢铵中的氢离子抑制水的电离,铵根离子水解促进水的电离,抑制作用更大,醋酸钠会促进水的电离,所以水电离出的c(H+):⑤>④>①>②,故B正确;
C、0.1mol/L的①氨水②盐酸等体积混合后生成氯化铵溶液,溶液中存在质子守恒:c(H+)=c(OH-)+c(NH3?H2O),故C错误;
D、氨水和氯化铵的混合液显示碱性,溶液中离子浓度的关系:c(NH4+)>c(Cl-)>c(OH-)>c(H+),故D错误.
故选B.
B、酸和碱对水的电离起抑制作用,盐酸的抑制作用大于氨水的抑制作用,能水解的盐对水的电离起促进作用,硫酸氢铵中的氢离子抑制水的电离,铵根离子水解促进水的电离,抑制作用更大,醋酸钠会促进水的电离,所以水电离出的c(H+):⑤>④>①>②,故B正确;
C、0.1mol/L的①氨水②盐酸等体积混合后生成氯化铵溶液,溶液中存在质子守恒:c(H+)=c(OH-)+c(NH3?H2O),故C错误;
D、氨水和氯化铵的混合液显示碱性,溶液中离子浓度的关系:c(NH4+)>c(Cl-)>c(OH-)>c(H+),故D错误.
故选B.
点评:本题考查学生弱电解质的电离平衡以及盐的水解等方面的知识,属于综合知识的考查,难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、淀粉和蛋白质它们水解的最终产物都是葡萄糖 |
| B、为防止轮船的船体在海水中被腐蚀,一般在船身连接锌块 |
| C、万一不慎误服重金属盐,应大量吞服鸡蛋清 |
| D、麦芽糖能水解,且最终水解产物有两种 |
下列关于Na2O和Na2O2的叙述正确的是( )
| A、都是白色固体 |
| B、都能和水反应形成强碱溶液 |
| C、都是碱性氧化物 |
| D、都是强氧化剂 |
进行化学实验、观察实验现象,通过分析、推理得出正确的结论是化学学习的方法之一.下列对有关实验事实的解释正确的是( )
| A、将N2和过量的O2在高温或放电的条件下反应得到红棕色的气体,说明NO为红棕色气体 |
| B、在AgNO3溶液中加入锌粉,能置换出银,说明Ag+的还原性比Zn2+强 |
| C、用干净的铂丝蘸取少量溶液在酒精灯外焰上灼烧,发现火焰呈黄色,则溶液中含Na+ |
| D、浓硫酸放入蔗糖中,能使蔗糖炭化,说明浓硫酸具有脱水性 |
下列说法正确的是( )
| A、海水中蕴含的元素有80多种,其中Mg、Br、I在海水中的总储量分别约为1.8×1015t、1×1014t、8×1010t.由于海水中镁的储量很大,工业上常以海水为原料提取镁,因此,镁元素被称为“海洋元素” |
| B、活泼金属元素的氧化物一定是碱性氧化物,非金属元素的氧化物一定是酸性氧化物 |
| C、氢氧化铁溶胶、甘油与乙醇的混合液、含PM2.5的大气均具有丁达尔效应 |
| D、绿色化学期望利用化学原理从源头消除污染,在化学过程中充分利用原料,实现零排放 |
下列说法正确的是( )
| A、放热的反应在常温下一定易进行 |
| B、吸热反应在常温下不能进行 |
| C、有吸热或放热现象的过程中一定发生了化学反应 |
| D、反应是放热还是吸热是由反应物和生成物所具有的能量的相对大小决定的 |
用如图装置进行的实验,不能达到相应实验目的是( )
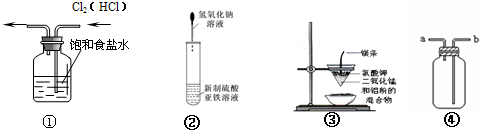

| A、装置①可除去Cl2中的HCl杂质 |
| B、装置②可用于制备氢氧化亚铁并观察其颜色 |
| C、装置③可制取金属锰 |
| D、装置④可用于收集H2、CO2、Cl2、HCl、NO2等气体 |
用1L 1.0mol/L NaOH溶液吸收0.8mol C02,所得溶液中含有( )
| A、C032- |
| B、HC03- |
| C、C032-和HC03- |
| D、C032-和OH- |
已知NH4CuSO3与足量的1mol?L-1硫酸溶液混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色.据此判断下列说法合理的是( )
| A、NH4CuSO3中硫元素被氧化了 |
| B、刺激性气味的气体是二氧化硫或氨气 |
| C、该反应中NH4CuSO3既是氧化剂又是还原剂 |
| D、该反应中硫酸既表现为酸性又表现氧化性 |