题目内容
奥运五环代表着全世界五大洲的人民团结在一起.下列各项中的物质能满足如图中阴影部分关系的是( )


| A、①NaCl;②K2SO4;③KCl;④(NH4)2SO4; |
| B、①Na2SO4;②K2SO4;③KCl;④(NH4)2SO4; |
| C、①NaCl;②K2SO4;③KCl;④NH4Cl; |
| D、①Na2SO4;②K2SO4;③KCl;④NH4Cl. |
考点:酸、碱、盐、氧化物的概念及其相互联系
专题:物质的分类专题
分析:根据盐电离出的阴阳离子的种类分类即可,例如阳离子为钠离子的盐统称为钠盐,阴离子为硫酸根离子的盐统称为硫酸盐.
解答:
解:A.①NaCl属于盐酸盐,不是硫酸盐,④(NH4)2SO4属于硫酸盐,不是盐酸盐,故A错误;
B.④(NH4)2SO4属于硫酸盐,不是盐酸盐,故B错误;
C.①NaCl属于盐酸盐,不是硫酸盐,故C错误;
D.Na2SO4属于钠盐和硫酸盐,K2SO4属于钾盐和硫酸盐,KCl属于盐酸盐和钾盐,NH4Cl属于铵盐和盐酸盐,各项均符合,故D正确;
故选D.
B.④(NH4)2SO4属于硫酸盐,不是盐酸盐,故B错误;
C.①NaCl属于盐酸盐,不是硫酸盐,故C错误;
D.Na2SO4属于钠盐和硫酸盐,K2SO4属于钾盐和硫酸盐,KCl属于盐酸盐和钾盐,NH4Cl属于铵盐和盐酸盐,各项均符合,故D正确;
故选D.
点评:本题考查了盐的分类,把握分类依据分析即可解答,题目难度不大.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目
下列各物质的名称正确的是( )
| A、1,2-二甲基丁烷 |
| B、2,3,3-三甲基-2-丁烯 |
| C、3,4,4-三甲基-1-戊炔 |
| D、2,3-二甲基苯 |
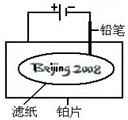 某学生设计了如图所示的“黑笔写红字”的趣味实验.滤纸上先用NaCl和无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹--“Beijing2008”. 据此,下列叙述不正确的是( )
某学生设计了如图所示的“黑笔写红字”的趣味实验.滤纸上先用NaCl和无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹--“Beijing2008”. 据此,下列叙述不正确的是( )| A、铅笔作阴极:电极反应为:2H++2e-=H2↑ | ||||
| B、铂片作阳极:电极反应为:2Cl--2e-=Cl2↑ | ||||
| C、铅笔与滤纸接触处有少量Cl2逸出 | ||||
D、上述反应总的离子方程式可表示为2Cl-+2H2O
|
下列说法正确的是( )
| A、海水中蕴含的元素有80多种,其中Mg、Br、I在海水中的总储量分别约为1.8×1015t、1×1014t、8×1010t.由于海水中镁的储量很大,工业上常以海水为原料提取镁,因此,镁元素被称为“海洋元素” |
| B、活泼金属元素的氧化物一定是碱性氧化物,非金属元素的氧化物一定是酸性氧化物 |
| C、氢氧化铁溶胶、甘油与乙醇的混合液、含PM2.5的大气均具有丁达尔效应 |
| D、绿色化学期望利用化学原理从源头消除污染,在化学过程中充分利用原料,实现零排放 |
正确掌握好化学用语是学好化学的基础,下列有关表述正确物是( )
| A、乙烯的结构简式:CH2CH2 |
B、NH3的电子式: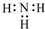 |
| C、NaHCO3水解的离子方程式:HCO3-+H2O?H3O++CO32- |
| D、亚硫酸氢根离子的电离方程式:HSO3-+H2O?H3O++SO32- |
用如图装置进行的实验,不能达到相应实验目的是( )
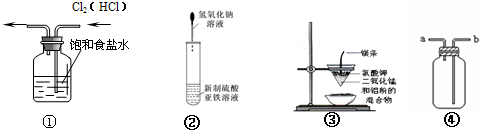

| A、装置①可除去Cl2中的HCl杂质 |
| B、装置②可用于制备氢氧化亚铁并观察其颜色 |
| C、装置③可制取金属锰 |
| D、装置④可用于收集H2、CO2、Cl2、HCl、NO2等气体 |
关于体积相同、pH均为3的H2SO4溶液和CH3COOH溶液,下列说法正确的是( )
| A、分别与足量的Mg反应,CH3COOH溶液产生的H2多 |
| B、分别用pH=12的NaOH溶液中和,H2SO4消耗的NaOH多 |
| C、分别加入对应的钠盐固体后,二者pH仍为3 |
| D、分别加水稀释100倍后,二者的pH均变为5 |
下列有关实验的操作正确的是( )
| A、容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 |
| B、检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
| C、为观察Mg条在CO2气体中的燃烧,在一个底部铺有少量玻璃棉的集气瓶中收集满 CO2气体,取一小段除去表面氧化膜的Mg条用坩埚钳夹持点燃后迅速投入上述集气瓶底部 |
| D、用干燥且洁净的玻璃棒蘸取NaClO溶液,滴到放在表面皿上的pH试纸上测pH值 |
在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从小到大的是( )
| A、p (Ne)<p (H2)<p (O2) |
| B、p (O2)<p (Ne)<p (H2) |
| C、p (H2)<p (O2)<p (Ne) |
| D、p (H2)<p (Ne)<p (O2) |