下列物质在水溶液中的电离方程式书写正确的是( )
| A、NaHSO4═Na++HSO4- |
| B、NaHCO3═Na++H++CO32- |
| C、CH3COOH═H++CH3COO- |
| D、NH3?H2O?NH4++OH- |
既与稀HCl反应,又与NaOH溶液反应的是( )
| A、Mg | B、Al | C、Fe | D、Cu |
现有一瓶乙二醇和丙三醇的均匀混合物,已知它们的性质如下表.据此,将乙二醇和丙三醇互相分离的最佳方法是( )
| 物质 | 分子式 | 熔点(0C) | 沸点(0C) | 密度(g.cm-3) | 溶解性 |
| 乙二醇 | C2H6O2 | -11.5 | 198 | 1.11 | 易溶于水和酒精 |
| 丙三醇 | C3H8O3 | 17.9 | 290 | 1.26 | 能与水酒精任意比互溶 |
| A、用水萃取出混和物中的丙三醇,再分液 |
| B、将混合物直接分液 |
| C、蒸馏法 |
| D、结晶法 |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、常温常压下,17g甲基(-14CH3)所含的中子数为9NA |
| B、pH=1的稀硫酸中含有的H+数为0.1NA |
| C、7.8g过氧化钠与足量二氧化碳反应转移的电子数为0.1NA |
| D、3molNO2和足量H2O反应,转移1NA个电子 |
 已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+.现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+.现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )| A、图中AB段的氧化剂为K2Cr2O7 |
| B、图中BC段发生的反应为2Fe3++2I-=2Fe2++I2 |
| C、开始加入的K2Cr2O7为0.25 mol |
| D、K2Cr2O7可与FeSO4反应的物质的量为1:3 |
对下列事实的解释正确的是( )
| A、常温下,将铜放入浓硫酸中无明显变化,说明铜在冷的浓硫酸中钝化 |
| B、浓硝酸在光照下变黄,证明硝酸不稳定,且产物有红棕色气体可溶于浓硝酸 |
| C、溴蒸气使湿润的碘化钾淀粉试纸变蓝,说明溴可与淀粉反应 |
| D、液氨是一种重要的制冷剂,说明氨气在液化时吸收大量的热 |
下列装置或操作合理的是( )


| A、装置①可用于实验室制取少量氯气 |
| B、装置②可用于实验室制取少量乙烯 |
| C、装置③可用于制备少量的乙酸乙酯 |
| D、装置④可用于比较碳酸与苯酚的酸性强弱 |
已知I-、Fe2+、Cl-、H2O2、SO2均有还原性,他们在酸性介质中还原性的强弱顺序为 Cl-<Fe2+<H2O2<I-<SO2,则下列反应不能发生的是( )
| A、2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
| B、I2+SO2+2H2O=H2SO4+2HI |
| C、H2O2+H2SO4=SO2↑+2H2O+O2↑ |
| D、2Fe2++I2=2Fe3++2I- |
下列说法正确的是( )
| A、常温下pH为5的盐酸溶液稀释1000倍后,pH等于8 |
| B、浓度均为0.1mol/L的氨水和氯化铵溶液,水电离出的c(H+)前者小于后者 |
| C、碳酸钠溶液中存在:c(Na+)+c(H+)=c(CO32-)+c(OH-)+c(HCO3-) |
| D、等浓度的CH3COOH与KOH以任意比混合:c(K+)+c(H+)=c(OH-)+c(CH3COO-) |
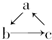 (“→”表示一步完成)关系转化的是( )
(“→”表示一步完成)关系转化的是( )