题目内容
下列各组物质中,不能按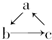 (“→”表示一步完成)关系转化的是( )
(“→”表示一步完成)关系转化的是( )
 (“→”表示一步完成)关系转化的是( )
(“→”表示一步完成)关系转化的是( )| 选项 | A | B | C | D |
| a | NaOH | HNO3 | HCl | S |
| b | Na2CO3 | NO | Cl2 | SO3 |
| c | NaCl | NO2 | HClO | H2SO4 |
| A、A | B、B | C、C | D、D |
考点:钠的重要化合物,硝酸的化学性质,氯、溴、碘及其化合物的综合应用,含硫物质的性质及综合应用
专题:元素及其化合物
分析:根据物质的性质进行判断,题中S在氧气中燃烧只生成SO2,SO2在催化剂作用下和氧气反应才可生成SO3.
解答:
解:A.可发生:NaOH
Na2CO3
NaHCO3
NaOH,可一步完成,故A不选;
B.可发生:HNO3
NO
NO2
HNO3,可一步完成,故B不选;
C.可发生:HCl
Cl2
HClO
HCl,可一步完成,故C不选;
D.S在氧气中燃烧只生成SO2,SO2在催化剂作用下和氧气反应才可生成SO3,不能一步完成,故D选.
故选D.
| CO2 |
| CO2 |
| Ca(OH)2 |
B.可发生:HNO3
| Cu |
| O2 |
| H2O |
C.可发生:HCl
| MnO2 |
| △ |
| H2O |
| 光照 |
D.S在氧气中燃烧只生成SO2,SO2在催化剂作用下和氧气反应才可生成SO3,不能一步完成,故D选.
故选D.
点评:本题考查元素化合物的性质,题目难度不大,本题注意常见元素化合物性质的积累.

练习册系列答案
相关题目
精制食盐水时下列物质中,不必用到的有( )
①NaOH溶液 ②盐酸 ③K2CO3溶液 ④BaCl2溶液 ⑤硫酸 ⑥Na2CO3溶液 ⑦Ba(NO3)2溶液.
①NaOH溶液 ②盐酸 ③K2CO3溶液 ④BaCl2溶液 ⑤硫酸 ⑥Na2CO3溶液 ⑦Ba(NO3)2溶液.
| A、③④⑤ | B、③⑤⑦ |
| C、②⑤⑥ | D、②④⑤⑦ |
下列离子方程式正确的是( )
| A、在碳酸氢钠溶液中加入等物质的量浓度等体积的氢氧化钠溶液:HCO3-+OH-=H2O+CO32- |
| B、硫酸铝溶液中加入过量氨水:Al3++4 NH3?H2O=AlO2-+4NH4++2H2O |
| C、硫酸与氢氧化钡溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D、碳酸钡溶于醋酸:BaCO3+2H+=Ba2++H2O+CO2↑ |
既与稀HCl反应,又与NaOH溶液反应的是( )
| A、Mg | B、Al | C、Fe | D、Cu |
关于焰色反应的叙述正确的是( )
| A、所有金属及其化合物在灼烧时都呈特征颜色 |
| B、进行焰色实验的铂丝用稀硫酸洗净后再蘸取样品灼烧 |
| C、透过蓝色钴玻璃观察钾元素的焰色是为了滤去黄光干扰 |
| D、金属钠在空气中燃烧发出黄光不是钠元素的焰色所致 |
强酸和强碱稀溶液的中和热可表示为( )
H+(aq)+OH-(aq)=H2O(l),△H=-57.3kJ/mol
①HCl(aq)+NH3?H2O(aq)=NH4Cl(aq)+H2O(l),△H=-akJ/mol
②HCl(aq)+NaOH(s)=NaCl(aq)+H2O(l),△H=-bkJ/mol
③Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l),△H=-ckJ/mol
则a,b,c三者的大小关系判断错误的是( )
H+(aq)+OH-(aq)=H2O(l),△H=-57.3kJ/mol
①HCl(aq)+NH3?H2O(aq)=NH4Cl(aq)+H2O(l),△H=-akJ/mol
②HCl(aq)+NaOH(s)=NaCl(aq)+H2O(l),△H=-bkJ/mol
③Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l),△H=-ckJ/mol
则a,b,c三者的大小关系判断错误的是( )
| A、c>114.6 |
| B、a<57.3 |
| C、b>57.3 |
| D、2a=2b=c |
将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应2A(g)+B(g)?2C(g),若经2s后测得C的浓度为0.6mol?L-1,现有下列几种说法,其中正确的是( )
| A、用物质A表示的反应的平均速率为0.3 mol?L-1?s-1 |
| B、用物质B表示的反应的平均速率为0.6 mol?L-1?s-1 |
| C、2s时物质A的转化率为70% |
| D、2s时物质B的体积分数为40% |