题目内容
下列说法正确的是( )
| A、常温下pH为5的盐酸溶液稀释1000倍后,pH等于8 |
| B、浓度均为0.1mol/L的氨水和氯化铵溶液,水电离出的c(H+)前者小于后者 |
| C、碳酸钠溶液中存在:c(Na+)+c(H+)=c(CO32-)+c(OH-)+c(HCO3-) |
| D、等浓度的CH3COOH与KOH以任意比混合:c(K+)+c(H+)=c(OH-)+c(CH3COO-) |
考点:弱电解质在水溶液中的电离平衡,离子浓度大小的比较,酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:A、酸溶液无限稀释溶液的pH接近于7;
B、碱对水的电离起抑制作用,能水解的盐对水的电离起促进作用;
C、溶液中存在电荷守恒;
D、CH3COOH与KOH反应得到的溶液中存在电荷守恒.
B、碱对水的电离起抑制作用,能水解的盐对水的电离起促进作用;
C、溶液中存在电荷守恒;
D、CH3COOH与KOH反应得到的溶液中存在电荷守恒.
解答:
解:A、常温下pH为5的盐酸溶液稀释1000倍后,溶液的pH接近于7,不会等于8,故A错误;
B、浓度为0.1mol/L的氨水对水的电离起抑制作用,浓度为0.1mol/L的氯化铵溶液是能水解的盐,对水的电离起促进作用,故B正确;
C、碳酸钠溶液中存在电荷守恒:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-),故C错误;
D、CH3COOH与KOH反应得到的溶液中存在电荷守恒:c(K+)+c(H+)=c(OH-)+c(CH3COO-),故D正确.
故选BD.
B、浓度为0.1mol/L的氨水对水的电离起抑制作用,浓度为0.1mol/L的氯化铵溶液是能水解的盐,对水的电离起促进作用,故B正确;
C、碳酸钠溶液中存在电荷守恒:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-),故C错误;
D、CH3COOH与KOH反应得到的溶液中存在电荷守恒:c(K+)+c(H+)=c(OH-)+c(CH3COO-),故D正确.
故选BD.
点评:本题考查学生弱电解质的电离平衡、溶液中的电荷守恒等知识,属于综合知识的考查,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
将a g铁和氧化铁的混合物加入800mL pH=1的盐酸中充分反应后,固体无剩余,盐酸全部消耗,放出标准状况下气体 0.224L.则下列判断中正确的是( )
| A、原混合物中n(Fe):n(Fe2O3)=2:1 |
| B、向溶液中滴入无色的KSCN溶液,显血红色 |
| C、无法计算出原混合物的质量 |
| D、此时溶液中Fe2+和Fe3+的物质的量之比为3:1 |
下列反应的离子方程式正确的是( )
| A、醋酸与锌粒反应:2H++Zn=H2↑+Zn2+ | ||||
| B、用FeCl3溶液腐蚀铜板:Cu+Fe3+=Cu2++Fe2+ | ||||
| C、向CaCl2溶液中通入少量CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+ | ||||
D、用石墨电极电解食盐水:2Cl-+2H2O
|
 已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+.现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+.现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )| A、图中AB段的氧化剂为K2Cr2O7 |
| B、图中BC段发生的反应为2Fe3++2I-=2Fe2++I2 |
| C、开始加入的K2Cr2O7为0.25 mol |
| D、K2Cr2O7可与FeSO4反应的物质的量为1:3 |
共价键、离子键、金属键、分子间作用力都是微粒间的作用力,含有以上两种作用力的晶体是( )
| A、HCl | B、金刚石 |
| C、NaOH | D、Na |
下列有关实验操作正确的是( )
A、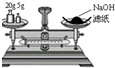 称量氢氧化钠固体 |
B、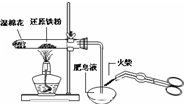 检验铁粉与水蒸气反应产生的氢气 |
C、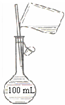 配制150 mL 0.10 mol/L盐酸 |
D、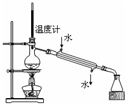 分离两种互溶但沸点相差较大的液体混合物 |
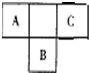 短周期元素的A、B、C在元素周期表中的位置如右图所示,已知A、C 两种元素的原子核外电子数之和等于B的质子数,B原子核内质子数和中子数相等.据此填空:
短周期元素的A、B、C在元素周期表中的位置如右图所示,已知A、C 两种元素的原子核外电子数之和等于B的质子数,B原子核内质子数和中子数相等.据此填空: