下列装置能达到实验目的是( )
A、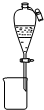 分离碘酒中的碘和酒精 |
B、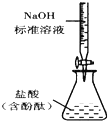 测定盐酸的浓度 |
C、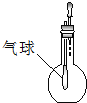 验证HCl的溶解性 |
D、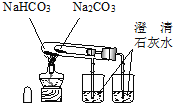 比较Na2CO3、NaHCO3的热稳定性 |
m g物质X、少量O2和过量Na2O2在密闭容器中加热,充分作用后固体增重m g.则关于X的下列说法不正确的是( )
| A、可能是纯净物,也可能是混合物 |
| B、分子通式为(CO)aH2b(a、b不同时为0或其它合理整数)的物质 |
| C、分子通式为Ca(H2O)b(a、b不同时为0或其它合理整数)的物质 |
| D、若X是CO和H2混合气体,CO和H2可按任意比例混合 |
下列判断不正确的是( )
①若NaA、NaB溶液的pH分别为9和8,则酸性一定是HA<HB;
②FeCl3溶液蒸干得FeCl3固体,Na2CO3溶液蒸干得Na2CO3固体;
③CH3COONa水解产生CH3COOH和OH-,向水解液中加入少量冰醋酸会因其中和OH-而使水解平衡右移;
④因Fe3++3H2O?Fe(OH)3+3H+,为抑制水解,配制FeCl3溶液时需将FeCl3溶解在稀H2SO4中;
⑤中和pH和体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同.
①若NaA、NaB溶液的pH分别为9和8,则酸性一定是HA<HB;
②FeCl3溶液蒸干得FeCl3固体,Na2CO3溶液蒸干得Na2CO3固体;
③CH3COONa水解产生CH3COOH和OH-,向水解液中加入少量冰醋酸会因其中和OH-而使水解平衡右移;
④因Fe3++3H2O?Fe(OH)3+3H+,为抑制水解,配制FeCl3溶液时需将FeCl3溶解在稀H2SO4中;
⑤中和pH和体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同.
| A、只有①②④⑤ | B、只有②③⑤ |
| C、只有①②③⑤ | D、全部 |
设某元素原子核内的质子数为12,质量数为24,则下述论断正确的是 ( )
| A、由此确定该元素的相对原子质量为24 |
| B、这种元素原子的近似相对原子质量为24 |
| C、若C-12原子质量为W g,此原子的质量约是为24W g |
| D、该原子核内中子的总质量近似等于质子的总质量 |
下列离子在溶液中能大量共存的是( )
| A、Fe3+、NH4+、SCN-、Cl- |
| B、Na+、H+、AlO2-、SO42- |
| C、Fe2+、Fe3+、Cl-、NO3- |
| D、Fe2+、NH4+、Cl-、OH- |
有人设想将不溶的碳酸盐材料通过特殊的加工方法使之变为纳米碳酸盐材料(即碳酸盐材料粒子直径是纳米级),这将使建筑材料的性能发生巨大变化,下列关于纳米碳酸盐材料的推测正确的是( )
| A、纳米碳酸盐材料是与胶体相似的分散系 |
| B、纳米碳酸盐材料分散到水中会产生丁达尔效应 |
| C、纳米碳酸盐材料的化学性质已与原来的碳酸盐材料完全不同 |
| D、纳米碳酸盐材料的粒子不能透过滤纸 |
下列各组物质中,不管它们以何种比例混合只要总质量一定,充分燃烧后生成的二氧化碳的质量不变的是( )
| A、乙炔和苯 |
| B、乙醇和丙醇(CH3CH2CH2OH) |
| C、乙酸和乙二醇(HOCH2-CH2OH) |
| D、甲醇CH3OH和乙酸 |
 合成氨工业对国民经济和社会发展具有重要的意义,对密闭容器中的反应:
合成氨工业对国民经济和社会发展具有重要的意义,对密闭容器中的反应:N2(g)+3H2(g)
| 催化剂 |
| 高温、高压 |
| A、点a的正反应速率比b点的大 |
| B、点c处反应还未达到平衡 |
| C、点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
| D、其他条件不变,500℃下反应至t1时刻,n(H2)比图中d点的值大 |