某单质能与足量浓HNO3反应放出NO2气体,若参加反应的单质和硝酸的物质的量之比为1:a,则该元素在反应中所显示的化合价是 ( )
| A、+2a | ||
| B、+a | ||
C、+
| ||
D、+
|
下列离子方程式不正确的是( )
| A、Na2CO3溶液与足量盐酸反应:CO32-+2H+═CO2↑+H2O |
| B、FeCl2溶液和Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
| C、钠与水反应:Na+H2O═Na++OH-+H2↑ |
| D、NaHCO3溶液与NaOH溶液:HCO3-+OH-═CO32-+H2O |
下列各组物质,不用任何化学试剂即可鉴别的是( )
| A、氯水、NaBr溶液、盐酸 |
| B、NaCl溶液、NaBr溶液、KI溶液 |
| C、氯化氢、溴化氢、碘化氢 |
| D、盐酸、NaCl溶液、AgNO3溶液、Na2CO3溶液 |
下列说法正确的是( )
| A、H与D,16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体;甲醇、乙二醇和丙三醇互为同系物 |
| B、在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 |
| C、HI的相对分子质量大于HF,所以HI的沸点高于HF |
| D、由IA族和VIA族元素形成的原子个数比为1:1、电子总数为38的化合物,是含有共价键的离子型化合物 |
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、1molNa2O2与足量的二氧化碳反应,转移电子的物质的量为2mol |
| B、等量的铝分别与足量的稀盐酸和氢氧化钠溶液反应生成氢气的质量相同 |
| C、含1mol HCl的盐酸溶液与足量Fe反应,Fe所失去的电子总数为0.5NA |
| D、标准状况下,11.2L H2O含有0.5NA个分子 |
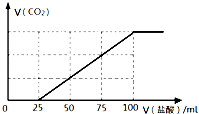 向100mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( )
向100mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( )| A、原NaOH溶液的浓度为0.2 mol/L |
| B、通入CO2的体积为448 mL |
| C、所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na2CO3)=1:3 |
| D、所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3)=1:1 |
下列物质中既能与盐酸反应,又能与NaOH溶液反应的是( )
①Na2SiO3; ②Al(OH)3; ③NH4HCO3; ④Al2O3.
①Na2SiO3; ②Al(OH)3; ③NH4HCO3; ④Al2O3.
| A、①②④ | B、②③④ |
| C、②④ | D、全部 |
下列有关除杂的操作不正确的是( )
| A、铁粉中混有少量铝粉:加入过量烧碱溶液,过滤 |
| B、碳酸氢钠粉末中含有少量碳酸钠粉末:加热 |
| C、除去FeCl3溶液中的FeCl2:加入氯水 |
| D、FeCl3药品中混有少量AlCl3:溶解、加入过量NaOH溶液过滤、将沉淀溶于盐酸 |
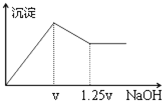 有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中c(Cl?)与c(SO42?)之比为( )
有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中c(Cl?)与c(SO42?)之比为( )| A、1:1 | B、2:3 |
| C、3:2 | D、2:1 |
 一定条件下,下列反应可为工业制盐酸、合成氨提供原料:CH4 (g)+H2O (g)?CO(g)+3H2(g)△H>0.当该反应达到平衡后,若仅改变图中x的量,重新达到平衡后,y值随x变化趋势合理的是( )
一定条件下,下列反应可为工业制盐酸、合成氨提供原料:CH4 (g)+H2O (g)?CO(g)+3H2(g)△H>0.当该反应达到平衡后,若仅改变图中x的量,重新达到平衡后,y值随x变化趋势合理的是( )