题目内容
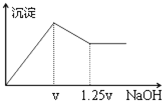 有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中c(Cl?)与c(SO42?)之比为( )
有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中c(Cl?)与c(SO42?)之比为( )| A、1:1 | B、2:3 |
| C、3:2 | D、2:1 |
考点:镁、铝的重要化合物,化学方程式的有关计算
专题:图示题
分析:设氢氧化钠物质的量浓度为1mol/L,首先发生反应Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓,然后发生反应Al(OH)3+OH-═AlO2-+2H2O,由图可知,溶解Al(OH)3消耗氢氧化钠溶液的体积为0.25V,物质的量为0.25Vmol,则n(Al3+)=0.25Vmol,根据离子方程式Al3++3OH-═Al(OH)3↓可知,沉淀Al3+消耗的氢氧化钠溶液的物质的量为0.25Vmol×3=0.75Vmol,沉淀Mg2+、Al3+总共消耗氢氧化钠溶液V,计算沉淀Mg2+消耗的氢氧化钠溶液的物质的量为Vmol-0.75molV=0.25Vmol,确定溶液中n(Mg2+)和n(Al3+),据此计算n(Cl-)与n(SO42?)进行解答.
解答:
解:设氢氧化钠物质的量浓度为1mol/L,首先发生反应Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓,然后发生反应Al(OH)3+OH-═AlO2-+2H2O,由图可知,溶解Al(OH)3消耗氢氧化钠溶液的体积为0.25V,物质的量为0.25Vmol,则n(Al3+)=0.25Vmol,根据离子方程式Al3++3OH-═Al(OH)3↓可知,沉淀Al3+消耗的氢氧化钠溶液的物质的量为0.25Vmol×3=0.75Vmol,沉淀Mg2+、Al3+总共消耗氢氧化钠溶液V,计算沉淀Mg2+消耗的氢氧化钠溶液的物质的量为Vmol-0.75molV=0.25Vmol,则n(Mg2+)=0.125Vmol,n(Cl-)=0.25Vmol;n(Al3+)=0.25Vmol,n(SO42-)=
n(Al3+)=
×0.25Vmol,溶液中c(Cl-):c(SO42-)=n(Cl-):n(SO42-)=0.25Vmol:
×0.25Vmol=2:3.
故选:B.
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
故选:B.
点评:本题考查镁铝化合物性质、混合物的有关计算,难度中等,清楚图象反应过程是解题关键.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B、标准状况下,11.2L甲醛气体中电子数为8NA |
| C、常温常压下,7.8g苯中含有单键的数目为0.6NA |
| D、1.0L0.1 mol?L-1 AlCl3溶液中所含的Al3+离子数为0.1NA |
某温度下,反应SO2(g)+
O2(g)?SO3 (g) 的平衡常数K1=100,在同一温度下,反应2SO3(g)?2SO2(g)+O2(g)的平衡常数K2的值为( )
| 1 |
| 2 |
| A、104 |
| B、200 |
| C、10-4 |
| D、10-2 |
下列溶液中不能通过化学反应区别SO2和CO2气体的是( )
| A、澄清石灰水 |
| B、KMnO4酸性溶液 |
| C、氯水 |
| D、品红溶液 |
关于下列各装置图的叙述中,不正确的是( )
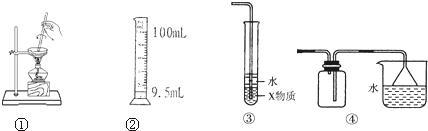

| A、装置①是把饱和食盐水中的食盐提取出来 |
| B、装置②用100mL量筒量取9.5mL液体 |
| C、装置③中X若为CCl4,可用于吸收NH3或HCl,并可防止倒吸 |
| D、装置④可用于收集NH3,并吸收多余的NH3 |
下列说法正确的是( )
| A、H与D,16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体;甲醇、乙二醇和丙三醇互为同系物 |
| B、在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 |
| C、HI的相对分子质量大于HF,所以HI的沸点高于HF |
| D、由IA族和VIA族元素形成的原子个数比为1:1、电子总数为38的化合物,是含有共价键的离子型化合物 |
下列表述正确的是( )
| A、向氯水中加入碳酸钙粉末,能提高溶液中HClO的浓度 |
| B、NH3是一种碱,能使湿润的红色石蕊试纸变蓝 |
| C、少量的CO2通入BaCl2溶液中会产生白色沉淀 |
| D、SO2能使酸性高锰酸钾溶液褪色,是因为SO2具有漂白性 |
下列化学用语正确的是( )
A、O2-的结构示意图: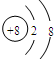 |
B、Na2S的电子式: |
C、羟基的电子式: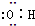 |
D、氮分子的结构式: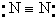 |