下列说法中正确的是( )
| A、氮气不活泼,所以氮元素的非金属性很弱 |
| B、铝原子比钠原子能失去较多的电子,所以铝有较强的金属性 |
| C、氟气通入水中有氧气生成说明水具有还原性 |
| D、二氧化硫能使品红溶液褪色说明它具有氧化性 |
下列做法正确的是( )
| A、不慎接触过多的氨,及时吸入新鲜的空气和水蒸气,并用大量水冲洗眼睛 |
| B、配制稀硫酸时,向浓硫酸中加入水进行稀释 |
| C、高锰酸钾加热制氧气实验结束时,不慎出现倒吸现象,应立即松开试管上的橡皮塞 |
| D、检验H2纯度时,用排空气法收集H2 |
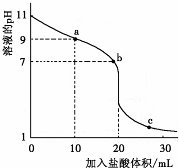 室温下,将0.1000mol?L-1盐酸滴入20.00mL 0.1000mol?L-1的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )
室温下,将0.1000mol?L-1盐酸滴入20.00mL 0.1000mol?L-1的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )| A、该一元碱的电离方程式为MOH=M++OH- |
| B、a、b、c三点中,c点水的电离程度最小 |
| C、室温下,MOH的电离常数Kb=1×10-5 |
| D、b点:c(M+)+c(MOH)=c(Cl-) |
下列说法正确的是( )
| A、已知常温下,物质的量浓度相等的CH3COONa与CH3COOH混合液的pH<7,在此溶液中继续加CH3COONa至pH=7,测得此时c(Na+)=0.1 mol?Lˉ1,则此时溶液中存在:c(Na+)=c(CH3COOˉ)>c(CH3COOH)>c(H+)=c(OHˉ) |
| B、0.01 mol?Lˉ1的Na2HPO4溶液中存在如下的平衡:HPO42ˉ+H2O?H2PO4ˉ+OHˉ HPO42ˉ?H++PO43ˉ且溶液pH>7;加水稀释后溶液中HPO43ˉ、PO43ˉ、H+的浓度均减小 |
| C、常温下,pH=6的盐酸和PH=6的NH4Cl溶液,其中水电离出的c(H+)值分别是xmol?L-1、y mol?L-1,两者关系是x>y |
| D、已知25℃时AgCl的Ksp=1.8×10-10,AgI的Ksp=9.5×l0-17,若在5mL含有KCl和KI各为0.0l mol?L-1的溶液中,加入8mL0.01 mol?L-1AgNO3溶液,这时溶液中所含溶质的离子浓度大小关系为c(NO3-)>c(K+)>c(Ag+)>c(Cl-)>c(I-) |
第七周期为不完全周期,若将来发现把这一周期元素全部排满,则下列有关第七周期元素的推论可能错误的是( )
| A、第七周期排满时有32种元素,全部是放射性元素 |
| B、第七周期排满时最后一种单质不与任何物质发生化学反应 |
| C、第七周期第ⅦA族元素的原子序数为117,是一种金属 |
| D、第七周期第ⅢA族元素的氢氧化物与Al(OH)3具有相似的化学性质 |
实验室制氮气,可用NaO2晶体与NH4Cl饱和溶液在加热的条件下发生如下反应:NaNO2+NH4Cl
NaCl+2H2O+N2↑,下列关于该反应的说法正确的是( )
| ||
| A、NaNO2是还原剂 |
| B、NH4Cl是氧化剂 |
| C、反应中有离子键、极性共价键和非极性共价键的断裂和形成 |
| D、每生成lmolN2,NaNO2得到3mol电子 |
下列分离或提纯物质的方法错误的是( )
| A、用加热的方法除去碳酸钠中含有的少量碳酸氢钠 |
| B、用过滤的方法提纯含有少量氯化铁的氢氧化铁胶体 |
| C、用溶解、过滤的方法除去碳酸钡中含有的少量硫酸钡 |
| D、用萃取的方法提取氯化钠溶液中的溴 |
某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g)?2C(g)达到平衡,测得平衡时A、B、C物质的量之比为n(A):n(B):n(C)=1:1:2,若保持温度不变,以1:1:2的物质的量之比再充入A、B、和C,下列判断中正确的是( )
| A、平衡不移动 |
| B、平衡向正反应方向移动 |
| C、新平衡时各物质的浓度都比原平衡时增大 |
| D、C的质量分数减小 |
质量相等的下列物质中分子数最少的是( )
| A、N2 |
| B、SO2 |
| C、SO3 |
| D、H2 |