题目内容
实验室制氮气,可用NaO2晶体与NH4Cl饱和溶液在加热的条件下发生如下反应:NaNO2+NH4Cl
NaCl+2H2O+N2↑,下列关于该反应的说法正确的是( )
| ||
| A、NaNO2是还原剂 |
| B、NH4Cl是氧化剂 |
| C、反应中有离子键、极性共价键和非极性共价键的断裂和形成 |
| D、每生成lmolN2,NaNO2得到3mol电子 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:NaNO2+NH4Cl
NaCl+2H2O+N2↑中,N元素的化合价由+3价降低为0,N元素的化合价由-3价升高为0,以此来解答.
| ||
解答:
解:A.由N元素的化合价降低可知NaNO2是氧化剂,故A错误;
B.由N元素的化合价升高可知NH4Cl是还原剂,故B错误;
C.反应物中没有非极性键的断裂,故C错误;
D.每生成lmolN2,由反应可知1molNaNO2得到1mol×(3-0)=3mol电子,故D正确;
故选D.
B.由N元素的化合价升高可知NH4Cl是还原剂,故B错误;
C.反应物中没有非极性键的断裂,故C错误;
D.每生成lmolN2,由反应可知1molNaNO2得到1mol×(3-0)=3mol电子,故D正确;
故选D.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,选项C为易错点,注意化学键的判断,题目难度不大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
一元酸HA溶液中,加入一定量强碱MOH溶液后,恰好完全反应,反应后的溶液中,下列判断正确的是( )
| A、c(A-)≥c(M+) |
| B、c(A-)≤c(M+) |
| C、c(OH-)<c(A-) |
| D、若MA水解,则c(OH-)>c(A-) |
对于2KI+Br2=2KBr+I2和2HBrO3+I2=2HIO3+Br2两反应,下列叙述不正确的是( )
| A、Br2的氧化性强于I2氧化性 | ||||
| B、I-的还原性强于Br-的还原性 | ||||
| C、I2的氧化性强于Br2的氧化性 | ||||
D、BrO
|
下列说法中正确的是( )
| A、氮气不活泼,所以氮元素的非金属性很弱 |
| B、铝原子比钠原子能失去较多的电子,所以铝有较强的金属性 |
| C、氟气通入水中有氧气生成说明水具有还原性 |
| D、二氧化硫能使品红溶液褪色说明它具有氧化性 |
由A、B两种气体组成的混合气体(A、B的相对分子质量分别为MA和MB),若A的质量分数为W%,则混合气体的平均相对分子质量是( )
A、
| ||||||
B、
| ||||||
| C、MA?W%+MB(1-W%) | ||||||
| D、无法确定 |
相同温度下,下列实验过程中,溶液的浓度和质量始终不变的是( )
| A、向98.3%浓H2SO4中加入ng SO3 |
| B、向浓氨水中持续通入干燥洁净的空气(已除去CO2) |
| C、向KNO3饱和溶液中加入ng KNO3晶体 |
| D、向CuSO4饱和溶液中加入ng无水CuSO4 |
用示意图或图示的方法能够直观形象地将化学知识传授给学生,下列示意图正确的是( )
A、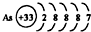 砷原子结构示意简图 |
B、 水合钠离子示意简图 |
C、 CO2分子示意图 |
D、 氧化还原反应与电子转移关系的示意图 |