被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰.在纸内的离子“流过”水和氧化锌组成的电解液.电池总反应为:Zn+2MnO2+H2O═ZnO+2MnO(OH).下列说法正确的是( )
| A、该电池的正极为锌 |
| B、该电池反应中二氧化锰起催化剂作用 |
| C、电池负极反应式为:Zn+2OH--2e-═ZnO+H2O |
| D、当 0.l mol Zn 完全溶解时,流经电解液的电子个数为1.204×l023 |
离子键的强弱主要决定于离子的半径和离子电荷值.一般规律是:离子半径越小,离子电荷值越大,则离子键越强.K2O、MgO、CaO三种物质中离子键由强到弱的顺序是( )
| A、K2O、MgO、CaO |
| B、MgO、K2O、CaO |
| C、MgO、CaO、K2O |
| D、CaO、MgO、K2O |
下列化学式的物质中只含有共价键是( )
| A、NaOH |
| B、Al2O3 |
| C、HCl |
| D、Ne |
某蓄电池放电、充电时反应为:Fe+Ni2O3+3H2O
Fe(OH)2+2Ni(OH)2,下列推断不正确的是( )
| 放电 |
| 充电 |
| A、放电时,负极上的电极反应式是:Fe+2OH--2e-=Fe(OH)2 |
| B、放电时,每转移2 mol 电子,正极上有1 mol Ni2O3被氧化 |
| C、充电时,阳极上的电极反应式是:2Ni(OH)2-2e-+2OH-=Ni2O3+3H2O |
| D、该蓄电池的电极必须是浸在某种碱性电解质溶液中 |
下列说法正确的是( )
| A、室温下,pH为11的氨水与pH为3的盐酸等体积混合,溶液呈中性 |
| B、在0.1 mol/L(NH4)2Fe(SO4)2溶液中:c(H+)+c(NH4+)+c(Fe2+)═c(OH-)+c(SO42-) |
| C、向醋酸溶液中加入适量醋酸钠,所得酸性溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、0.2mo1?L-1的Na2CO3溶液:c(OH-)═c(HCO3-)+c(H+)+2c(H2CO3) |
25℃时,下列有关溶液中微粒的物质的量浓度关系不正确的是( )
| A、0.1 mol?L-1 (NH4)2Fe(SO4)2溶液中:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+) |
| B、pH=11的氨水和pH=3的盐酸溶液等体积混合,所得溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C、0.1 mol?L-1 CH3COONa溶液中:c(CH3COO-)+c(CH3COOH)=0.1 mol?L-1 |
| D、0.1 mol?L-1的醋酸钠溶液20 mL与0.1 mol?L-1盐酸10 mL混合后溶液显酸性:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
下列溶液中各微粒的浓度关系或说法正确的是( )
| A、0.1 mol?L-1 pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) |
| B、等物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、 ④NH3?H2O;c(NH4+) 由大到小的顺序是:①>②>③>④ |
| C、a mol?L-1HCN溶液与b mol?L-1NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b |
| D、0.1mol?L-1的醋酸的pH=a,0.01mol?L-1的醋酸的pH=b,则a+1=b |
随着卤素原子半径的增大,下列递变规律正确的是( )
| A、单质的熔、沸点逐渐降低 |
| B、卤素离子的还原性逐渐增强 |
| C、单质的氧化性逐渐增强 |
| D、气态氢化物的稳定性逐渐增强 |
在25℃时浓度分别为a、b、c(mol/L)的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2(硫酸亚铁铵)三种溶液中,测得其中NH4+的物质的量的浓度相等,则下列判断正确的是( )
| A、a>b>c |
| B、c>a>b |
| C、a>c>b |
| D、b>a>c |
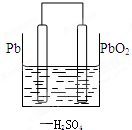 (1)铅蓄电池在生产生活中有广泛的应用,其工作原理为总方程式:Pb+PbO2+2H2SO4═2PbSO4+2H2O,其中负极为
(1)铅蓄电池在生产生活中有广泛的应用,其工作原理为总方程式:Pb+PbO2+2H2SO4═2PbSO4+2H2O,其中负极为