现有200mL MgCl2和AlCl3的混合溶液,其中c(Mg2+)=0.2mol/L,c(Cl-)=1.3mol/L,要使Mg2+转化成Mg(OH)2,并使Mg2+、Al3+分离开来,4mol/L NaOH溶液的最少用量为( )
| A、140mL | B、120mL |
| C、100mL | D、80mL |
电解100mL 16%的氢氧化钠溶液(密度为1g/cm3),用石墨作电极,10min后电解液的浓度为19.5%,这是因为( )
| A、溶质增加了3.5g |
| B、氢氧化钠的物质的量不变,而水被电解了1mol |
| C、氢氧化钠的消耗比水的消耗少 |
| D、氢氧化钠不参加反应,只有水参加反应,且放出H2和O2,消耗了18g水 |
向FeCl3和CuCl2混合液中加入过量的铁粉,反应完毕后,剩下的固体物质恰好跟加入的铁粉质量相等,则原混合液中FeCl3和CuCl2物质的量之比为( )
| A、2:7 | B、7:2 |
| C、1:7 | D、7:1 |
下列说法正确的是( )
| A、中和热一定是强酸跟强碱反应放出的热量 |
| B、1 mol酸与1 mol碱完全反应放出的热量是中和热 |
| C、在稀溶液中,酸与碱发生中和反应生成1 mol H2O(l)时的反应热叫做中和热 |
| D、测定中和热时可用稀硫酸和稀Ba(OH)2溶液 |
下列说法正确的是( )
| A、物质发生化学反应都伴随着能量变化 |
| B、伴有能量变化的物质变化都是化学变化 |
| C、在一个化学反应中,反应物的总能量与生成物的总能量一定相同 |
| D、在一个化学反应中,反应物的总能量一定高于生成物的总能量 |
阿伏加德罗常数约为6.02×1023mol-1,下列说法中正确的是( )
| A、22.4 L CH3CHO中含有的分子数约为6.02×1023 |
| B、56g铁与稀HNO3充分反应,转移电子数为0.3NA |
| C、常温常压下,由6 g NO2和40 g N2O4组成的混合气体中原子总数约为3×6.02×1023 |
| D、80 g NH4NO3晶体中含有NH4+小于 6.02×1023个 |
在一定条件下,将2mol A和1mol B混合于固定容积为2L的密闭容器中,发生如下反应:
,5s时测得气体压强是反应前的
,此段时间内C的平均生成率为( )
| 3A(g)+B(g) |
| xC(g)+2D(g) |
| 5 |
| 6 |
| A、0.25mol/L/s |
| B、0.1 |
| C、0.05mol/(L?s) |
| D、条件不足,无法计算 |
下列说法中正确的是( )
| A、为了快速配制好溶液,可以用容量瓶直接溶解氯化钠固体来配制溶液 |
| B、Cu中混有CuO,可以通过加入足量盐酸溶液,再过滤、洗涤烘干可得到洁净的Cu |
| C、设NA为阿伏伽德罗常数的值,1.0 L c(H+)=1.0mol/L的硫酸溶液中含有的H+数为NA |
| D、Fe(OH)3胶体是能产生丁达尔效应的分散系,而CuSO4溶液和蒸馏水是不能产生丁达尔效应的分散系 |
一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g)?xC(g)△H<0,B、C的物质的量随时间变化的关系如图1,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2
下列有关说法正确的是( )
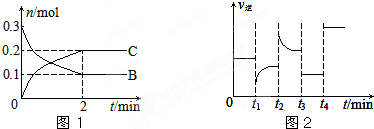
下列有关说法正确的是( )

| A、x=2,反应开始2 min内,v(B)=0.1 mol/(L?min) |
| B、t3时可能是减小压强,平衡不移动;t4时可能是使用催化剂,c(B)不变 |
| C、t2时改变的条件可能是增大c(C),B的转化率增大 |
| D、t1时改变的条件可能是降温,A(s)的质量增加 |