题目内容
在一定条件下,将2mol A和1mol B混合于固定容积为2L的密闭容器中,发生如下反应:
,5s时测得气体压强是反应前的
,此段时间内C的平均生成率为( )
| 3A(g)+B(g) |
| xC(g)+2D(g) |
| 5 |
| 6 |
| A、0.25mol/L/s |
| B、0.1 |
| C、0.05mol/(L?s) |
| D、条件不足,无法计算 |
考点:反应速率的定量表示方法
专题:化学反应速率专题
分析:依据化学平衡三段式列式计算,气体物质的量之比等于压强之比计算,反应速率v=
得到.
| △c |
| △t |
解答:
解:在一定条件下,将2mol A和1mol B混合于固定容积为2L的密闭容器中,发生如下反应,3A(g)+B(g)=xC(g)+2D(g),设反应中B消耗物质的量为m,则
3A(g)+B(g)=xC(g)+2D(g),
起始量(mol/L) 2 1 0 0
变化量(mol/L) 3m m xm 2m
平衡量(mol/L)2-3m 1-m xm 2m
5s时测得气体压强是反应前的
,气体体积减小3+1>x+2,x<2,x只能为1;
气体物质的量之比等于压强之比,2-3m+1-m+m+2m=
×3
m=0.5mol,此段时间内C的平均生成率=
=0.05mol/(L?s),
故选C.
3A(g)+B(g)=xC(g)+2D(g),
起始量(mol/L) 2 1 0 0
变化量(mol/L) 3m m xm 2m
平衡量(mol/L)2-3m 1-m xm 2m
5s时测得气体压强是反应前的
| 5 |
| 6 |
气体物质的量之比等于压强之比,2-3m+1-m+m+2m=
| 5 |
| 6 |
m=0.5mol,此段时间内C的平均生成率=
| ||
| 5s |
故选C.
点评:本题考查了化学平衡计算方法和反应速率概念的计算应用,主要是三段式计算和化学方程式计量数确定,题目较简单.

练习册系列答案
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
相关题目
下列做法中不符合“绿色化学”思想的是( )
| A、以水性涂料代替油性涂料 |
| B、以无磷洗涤剂代替含磷洗涤剂 |
| C、实验后的有毒有害物质应分类收集、统一处理 |
| D、在通风橱中制氯气时不用NaOH溶液吸收尾气 |
向FeCl3和CuCl2混合液中加入过量的铁粉,反应完毕后,剩下的固体物质恰好跟加入的铁粉质量相等,则原混合液中FeCl3和CuCl2物质的量之比为( )
| A、2:7 | B、7:2 |
| C、1:7 | D、7:1 |
只用一种试剂,区别甲苯,四氯化碳,己烯,乙醇,碘化钾溶液,亚硫酸6种无色溶液,应选用( )
| A、酸性KMnO4溶液 |
| B、溴水 |
| C、碘水 |
| D、硝酸银溶液 |
全轨电池以惰性材料作电极,在电解质溶液中发生的电池总反应为:VO2+(蓝色)+H2O+V3+(紫色)
VO2+(黄色)+V2+(绿色)+2H+下列说法错误的是( )
| 充电 |
| 放电 |
| A、充电时,阳极附近溶液由蓝色逐渐变为黄色 |
| B、放电过程中,正极附近溶液的酸性减弱 |
| C、充电时,反应每生成2mol H+时电子转移数为2mol |
| D、放电时,正极反应为VO2++2H++e-═VO2++H2O |
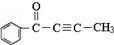 的有机物分子中:在同一直线上的碳原子最多有
的有机物分子中:在同一直线上的碳原子最多有