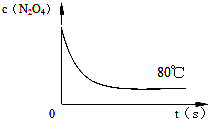
某兴趣小组为探究外界条件对可逆反应A(g)+B(g)═C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10L的密闭容器中充入1mol A和1mol B,反应达平衡时测得容器中各物质的浓度为Ⅰ.然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为Ⅱ、Ⅲ、Ⅳ.
针对上述系列实验,下列结论中错误的是( )
| A | B | C | |
| Ⅰ | 0.050mol?L-1 | 0.050mol?L-1 | 0.050mol?L-1 |
| Ⅱ | 0.070mol?L-1 | 0.070mol?L-1 | 0.098mol?L-1 |
| Ⅲ | 0.060mol?L-1 | 0.060mol?L-1 | 0.040mol?L-1 |
| Ⅳ | 0.080mol?L-1 | 0.080mol?L-1 | 0.12mol?L-1 |
| A、由Ⅰ中数据可计算出该温度下反应的平衡常数K=20mol-1?L |
| B、Ⅱ可能是通过增大C的浓度实现的 |
| C、若Ⅲ只是升高温度,则与Ⅰ比较,可以判断出正反应一定是放热反应 |
| D、第Ⅳ组实验数据的得出,只能通过压缩容器的体积才可以实现 |
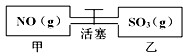 如图,容积相等的甲乙两个容器,通过活塞相连,分别充入NO和SO3且使气体密度相等.打开活塞使气体充分混合,发生反应:SO3(g)+NO(g)?SO2(g)+NO2(g)并达到平衡.反应过程中两容器的温度恒定且相等.则打开活塞前后,容器甲中保持不变的是( )
如图,容积相等的甲乙两个容器,通过活塞相连,分别充入NO和SO3且使气体密度相等.打开活塞使气体充分混合,发生反应:SO3(g)+NO(g)?SO2(g)+NO2(g)并达到平衡.反应过程中两容器的温度恒定且相等.则打开活塞前后,容器甲中保持不变的是( )| A、气体的密度 |
| B、气体分子数 |
| C、气体压强 |
| D、气体平均摩尔质量 |
可逆反应 H2 (g)+I2 (g)?2HI(g),温度一定,在1L的密闭容器中加入2molH2(g)和1molI2(g)开始反应,2min末测知容器中生成了1.2mol HI(g),下列说法正确的是( )
| A、H2(g)的消耗速率与I2(g)的生成速率始终相等 |
| B、反应过程中,H2(g)和I2(g)的转化率始终相等 |
| C、平衡前,正、逆反应速率的比值恒定 |
| D、反应开始至2min末,v(H2)=0.3mol?L-1?min-1 |
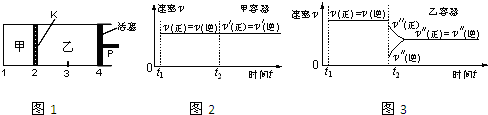
(双选)一定温度下可逆反应:A(s)+2B(g)?2C(g)+D(g);△H<0.现将1mol A和2mol B加入甲容器中,将4mol C和2mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动).下列说法正确的是( )

| A、保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| B、保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增大 |
| C、保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
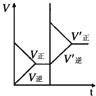
| D、保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
下列说法不正确的是( )
| A、油脂是高级脂肪酸的甘油酯 |
| B、油脂与氢气发生加成反应,可以得到硬化油 |
| C、油脂在酸性条件或碱性条件下,可以发生皂化反应 |
| D、日常使用的花生油、豆油、动物油都是油脂,它们可以溶解一些脂溶性维生素 |
可确认发生了化学平衡移动的是( )
| A、由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变 |
| B、有气态物质参加的可逆反应达到平衡后,改变了压强 |
| C、化学反应速率发生了改变 |
| D、可逆反应达到平衡后,使用催化剂 |
 平衡密闭容器中,加入一定量的X和Y,发生如下反应:2X(?)+Y(?)?2Z(?),不同温度时产物Z的生成情况如图所示:a为T1℃时的情况,b为T2℃时的情况,c为T2℃时从时间t3开始向容器中加压的情况.下列叙述正确的是( )
平衡密闭容器中,加入一定量的X和Y,发生如下反应:2X(?)+Y(?)?2Z(?),不同温度时产物Z的生成情况如图所示:a为T1℃时的情况,b为T2℃时的情况,c为T2℃时从时间t3开始向容器中加压的情况.下列叙述正确的是( )| A、X、Y、Z均为气体,正反应放热 |
| B、Y、Z为气体,X为非气体,正反应放热 |
| C、Z为气体,X、Y中至少有一种为非气体,正反应放热 |
| D、t4时刻气体的平均相对分子质量可能小于t3时刻气体的平均相对分子质量 |