题目内容
在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅.
(1)该反应的化学方程式为 .
(2)20s时,N2O4的浓度为 mol?L-1,0~20s内N2O4的平均反应速率为
(3)该反应的平衡常数表达式K= ,80℃反应K值为 保留2位小数)
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时 .
A.N2O4的转化率越高 B.NO2的产量越大
C.N2O4与NO2的浓度之比越大 D.正反应进行的程度越大
(5)要增大该反应的K值,可采取的措施
A.增大N2O4起始浓度 B.向混合气中通入NO2
C.使用高效催化剂 D.升高温度
(6)如图是80℃时容器中N2O4浓度的变化图,请在该图中补画出该反应在60℃反应时N2O4浓度的变化曲线.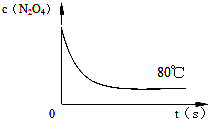
时间 (s) c(mol?L-1) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4) | 0.20 | a | 0.10 | C | d | e |
| c(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
(1)该反应的化学方程式为
(2)20s时,N2O4的浓度为
(3)该反应的平衡常数表达式K=
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时
A.N2O4的转化率越高 B.NO2的产量越大
C.N2O4与NO2的浓度之比越大 D.正反应进行的程度越大
(5)要增大该反应的K值,可采取的措施
A.增大N2O4起始浓度 B.向混合气中通入NO2
C.使用高效催化剂 D.升高温度
(6)如图是80℃时容器中N2O4浓度的变化图,请在该图中补画出该反应在60℃反应时N2O4浓度的变化曲线.

考点:化学平衡建立的过程,化学平衡常数的含义,化学平衡的影响因素
专题:化学平衡专题
分析:(1)依据图表数据分析,反应物和生成物分析判断;
(2)化学平衡的三段式列式计算,结合化学反应速率概念计算0~20s内N2O4的平均反应速率;
(3)依据化学方程式和平衡常数概念写出平衡常数表达式,依据80°C平衡状态下结合三段式列式计算平衡浓度计算平衡常数;
(4)根据平衡常数的定义可知,K值越大,生成物浓度越大,反应物浓度越小,则反应正向进行的程度越大,据此答题;
(5)要增大该反应的K值,就是要使平衡正向移动,且平衡常数只与温度有关,根据影响平衡常数的外界因素可以作判断;
(6)根据温度对化学反应速率和化学平衡的影响
(2)化学平衡的三段式列式计算,结合化学反应速率概念计算0~20s内N2O4的平均反应速率;
(3)依据化学方程式和平衡常数概念写出平衡常数表达式,依据80°C平衡状态下结合三段式列式计算平衡浓度计算平衡常数;
(4)根据平衡常数的定义可知,K值越大,生成物浓度越大,反应物浓度越小,则反应正向进行的程度越大,据此答题;
(5)要增大该反应的K值,就是要使平衡正向移动,且平衡常数只与温度有关,根据影响平衡常数的外界因素可以作判断;
(6)根据温度对化学反应速率和化学平衡的影响
解答:
解:(1)将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,反应的化学方程式为N2O4?2NO2,故答案为:N2O4?2NO2;
(2)进行到20S;
N2O4?2NO2
起始量(mol) 0.4 0
变化量(mol) 0.12 0.24
20S末(mol) 0.28 0.24
20s时,N2O4的浓度=
=0.14mol/L;
0~20s内N2O4的平均反应速率=
=0.003mol/(L?s);
故答案为:0.14;0.003mol/(L?s);
(3)N2O4?2NO2,平衡常数K=
,
80°C平衡状态和60S是相同平衡状态,平衡浓度c(NO2)=0.22mol/L,c(N2O4)=0.09mol/L;
平衡常数K=
═
=0.54,
故答案为:
;0.54;
(4)N2O4?2NO2
根据平衡常数的定义可知,K值越大,生成物浓度越大,反应物浓度越小,则反应正向进行的程度越大,
A.反应正向进行,K值越大,N2O4的转化率越高,故A正确
B.反应正向进行,K值越大,NO2的产量越大,故B正确;
C.K值越大,生成物浓度越大,反应物浓度越小,N2O4与NO2的浓度之比越小,故C错误;
D.K值越大,生成物浓度越大,反应物浓度越小,则反应正向进行的程度越大,故D正确;
故答案为:ABD.
(5)要增大该反应的K值,就是要使平衡正向移动,且平衡常数只与温度有关,根据影响平衡常数的外界因素可知,只有D正确;
故选D;
(6)应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅.说明降温平衡逆向进行,逆反应为放热反应,正反应为吸热反应,
温度降低,化学反应速率减慢,到达平衡的时间长,同时,温度降低,化学平衡向放热的方向移动,即逆反应方向移动,60℃反应时N2O4浓度的变化的曲线
如右图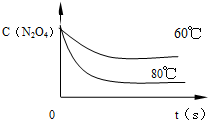
故答案为: ;
;
(2)进行到20S;
N2O4?2NO2
起始量(mol) 0.4 0
变化量(mol) 0.12 0.24
20S末(mol) 0.28 0.24
20s时,N2O4的浓度=
| 0.28mol |
| 2L |
0~20s内N2O4的平均反应速率=
| ||
| 20s |
故答案为:0.14;0.003mol/(L?s);
(3)N2O4?2NO2,平衡常数K=
| c2(NO2) |
| c(N2O4) |
80°C平衡状态和60S是相同平衡状态,平衡浓度c(NO2)=0.22mol/L,c(N2O4)=0.09mol/L;
平衡常数K=
| c2(NO2) |
| c(N2O4) |
| 0.222 |
| 0.09 |
故答案为:
| c2(NO2) |
| c(N2O4) |
(4)N2O4?2NO2
根据平衡常数的定义可知,K值越大,生成物浓度越大,反应物浓度越小,则反应正向进行的程度越大,
A.反应正向进行,K值越大,N2O4的转化率越高,故A正确
B.反应正向进行,K值越大,NO2的产量越大,故B正确;
C.K值越大,生成物浓度越大,反应物浓度越小,N2O4与NO2的浓度之比越小,故C错误;
D.K值越大,生成物浓度越大,反应物浓度越小,则反应正向进行的程度越大,故D正确;
故答案为:ABD.
(5)要增大该反应的K值,就是要使平衡正向移动,且平衡常数只与温度有关,根据影响平衡常数的外界因素可知,只有D正确;
故选D;
(6)应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅.说明降温平衡逆向进行,逆反应为放热反应,正反应为吸热反应,
温度降低,化学反应速率减慢,到达平衡的时间长,同时,温度降低,化学平衡向放热的方向移动,即逆反应方向移动,60℃反应时N2O4浓度的变化的曲线
如右图

故答案为:
 ;
;
点评:本题考查了化学反应速率的计算、化学平衡常数的含义、化学图象分析和绘制等知识点,注意化学平衡常数只与温度有关,与物质的浓度无关,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某有机物完全燃烧,生成的产物只有CO2和H2O.将6g该有机物完全燃烧的产物通过浓硫酸,浓硫酸增重7.2g,再通过氢氧化钠溶液,又增重13.2g.该有机物的分子式为( )
| A、C4H10 |
| B、C3H8 |
| C、C3H8O |
| D、C2H4O2 |
 平衡密闭容器中,加入一定量的X和Y,发生如下反应:2X(?)+Y(?)?2Z(?),不同温度时产物Z的生成情况如图所示:a为T1℃时的情况,b为T2℃时的情况,c为T2℃时从时间t3开始向容器中加压的情况.下列叙述正确的是( )
平衡密闭容器中,加入一定量的X和Y,发生如下反应:2X(?)+Y(?)?2Z(?),不同温度时产物Z的生成情况如图所示:a为T1℃时的情况,b为T2℃时的情况,c为T2℃时从时间t3开始向容器中加压的情况.下列叙述正确的是( )| A、X、Y、Z均为气体,正反应放热 |
| B、Y、Z为气体,X为非气体,正反应放热 |
| C、Z为气体,X、Y中至少有一种为非气体,正反应放热 |
| D、t4时刻气体的平均相对分子质量可能小于t3时刻气体的平均相对分子质量 |
有一容积固定的密闭反应器,中间有一个可自由移动的导热的隔板将容器分成甲、乙两部分,分别发生下列两个可逆反应:
甲 乙
乙
甲:a(g)+b(g)?2c(g)△H1<0 乙:x(g)+3y(g)?2z(g)△H2>0
起初甲、乙均达到反应平衡后隔板位于正中间,然后进行相关操作后,下列叙述错误的是( )
甲
 乙
乙甲:a(g)+b(g)?2c(g)△H1<0 乙:x(g)+3y(g)?2z(g)△H2>0
起初甲、乙均达到反应平衡后隔板位于正中间,然后进行相关操作后,下列叙述错误的是( )
| A、绝热下向甲中通入惰性气体,c的物质的量不变 |
| B、绝热下向乙中通入z气体,反应器中温度升高 |
| C、恒温下向甲中通入惰性气体,甲中平衡不移动,乙中X、Y的转化率增大 |
| D、恒温下向乙中通入z气体,y的物质的量浓度增大 |
据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实,其反应的化学方程式为:2CO2(g)+6H2(g)═CH3CH2OH(g)+3H2O(g).下列叙述正确的是( )
| A、当v(CO2)=2v(CH3CH2OH)时,反应一定达到平衡状态 |
| B、增大压强,可提高CO2和H2的转化率 |
| C、当平衡向正反应方向移动时,平衡常数一定增大 |
| D、移去生成的乙醇和水,可以加快反应速率 |
完成下列实验,所选装置正确的是( )
| A | B | C | D | |
| 实验 目的 | 实验室 制备乙烯 | 分离苯和溴苯的混合物(沸点:苯为80.1℃,溴苯为156.2℃) | 分离KCl和NH4Cl固体混合物 | 实验室用纯碱和稀硫酸制备二氧化碳 |
| 实验装置 |  |  | 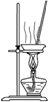 | 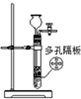 |
| A、A | B、B | C、C | D、D |
在元素周期表中,对于相同主族相邻周期的两种元素原子序数之差的叙述正确的是( )
| A、第2、3周期两元素相差均为8 |
| B、第3、4周期两元素相差均为18 |
| C、第5、6周期两元素相差均为32 |
| D、以上叙述均正确 |