题目内容
下列研究目的和示意图相符的是( )
| A | B | C | D | |
| 研 究 目 的 | 固定容积的密闭容器中,压强对反应: 2SO2(g)+O2(g)?2SO3(g)的影响 | 固定容积的密闭容器中,温度对反应: N2(g)+3H2(g)?2NH3(g)△H<0的影响 | 固定容积的密闭容器中,增大CO2浓度,对已达平衡的反应: CO(g)+H2O(g)?CO2(g)+H2(g)的影响 | 等质量Na、K 分别与足量水反应 |
| 示 意 图 | 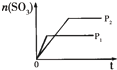 | 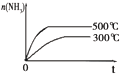 | 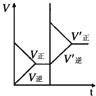 | 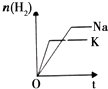 |
| A、A | B、B | C、C | D、D |
考点:化学平衡建立的过程
专题:化学平衡专题
分析:A、依据先拐先平压强大,结合三氧化硫含量随压强变化和平衡移动原理分析判断;
B、依据先拐先平温度大,结合氨气物质的量随温度变化和平衡移动原理分析;
C、增大二氧化碳浓度,平衡逆向进行,逆反应速率瞬间增大,正反应速率瞬间不变;
D、等质量钾和钠,与水反应钾生成的氢气少,但钾活泼性大于钠,反应快;
B、依据先拐先平温度大,结合氨气物质的量随温度变化和平衡移动原理分析;
C、增大二氧化碳浓度,平衡逆向进行,逆反应速率瞬间增大,正反应速率瞬间不变;
D、等质量钾和钠,与水反应钾生成的氢气少,但钾活泼性大于钠,反应快;
解答:
解:A、依据先拐先平压强大,P1>P2,三氧化硫含量随压强增大而增大,图象变化中不符合,故A错误;
B、依据先拐先平温度大,反应是放热反应,升温平衡逆向进行,氨气物质的量减小,图象中不符合,故B错误;
C、增大二氧化碳浓度,平衡逆向进行,逆反应速率瞬间增大,正反应速率瞬间不变,图象中改变条件正反应方向进行不符合,故C错误;
D、等质量钾和钠,钾没摩尔质量为39g/mol,钠摩尔质量为23g/mol,依据电子守恒可知与水反应,钾生成的氢气少,但钾活泼性大于钠,反应快先反应完,图象符合,故D正确;
故选D.
B、依据先拐先平温度大,反应是放热反应,升温平衡逆向进行,氨气物质的量减小,图象中不符合,故B错误;
C、增大二氧化碳浓度,平衡逆向进行,逆反应速率瞬间增大,正反应速率瞬间不变,图象中改变条件正反应方向进行不符合,故C错误;
D、等质量钾和钠,钾没摩尔质量为39g/mol,钠摩尔质量为23g/mol,依据电子守恒可知与水反应,钾生成的氢气少,但钾活泼性大于钠,反应快先反应完,图象符合,故D正确;
故选D.
点评:本题考查了化学平衡影响因素分析判断,图象分析方法和特征理解应用,掌握基础和平衡移动原理是关键,题目难度中等.

练习册系列答案
相关题目
可确认发生了化学平衡移动的是( )
| A、由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变 |
| B、有气态物质参加的可逆反应达到平衡后,改变了压强 |
| C、化学反应速率发生了改变 |
| D、可逆反应达到平衡后,使用催化剂 |
相同温度下,容积相同的甲、乙、丙3个恒容密闭容器中发生可逆反应:2SO2(g)+O2(g)?2SO3(g);△H=-197kJ?mol-1.实验测得起始、平衡时的有关数据如表所示,下列叙述正确的是( )
| 容器 | 起始各物质的物质的量/mol | 达到平衡时体系 能量的变化 | |||
| SO2 | O2 | SO3 | Ar | ||
| 甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2 |
| 丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
| A、Q1=Q2=Q3=197kJ |
| B、若在上述条件下反应生成2mol SO3(s)的反应热为△H1,则△H1>-197kJ?mol-1 |
| C、甲、乙、丙3个容器中反应的平衡常数不相等 |
| D、达到平衡时,丙容器中SO2的体积分数最小 |
一定温度下,将2mol PCl3和 1mol Cl2充入容积不变的密闭容器中,在一定条件下反应:PCl3+Cl2?PCl5,各物质均为气态.达平衡后,PCl5为0.4mol.若此时再加入1molPCl3 和0.5molCl2,相同温度下达到平衡,PCl5的物质的量为x( )
| A、0.4mol |
| B、0.6mol |
| C、0.4<x<0.6mol |
| D、x>0.6mol |
Mg和Al都是较活泼的金属,下列说法正确的是( )
A、Mg+2RbCl
| ||||
| B、在由镁铝形成的原电池中,负极反应一定是:Mg-2e-═Mg2+ | ||||
| C、MgCl2、AlCl3溶液分别加热蒸发、灼烧,均可得到氧化镁和氧化铝 | ||||
| D、因为氧化镁和氧化铝都是高熔点的物质,所以工业上分别用电解熔融MgCl2和AlCl3的方法制取镁和铝 |
 开发新型储氢材料是氢能利用的重要研究方向.
开发新型储氢材料是氢能利用的重要研究方向. 可以被氧化为
可以被氧化为 ,根据已知信息,试回答分子式是C4H10O的醇可被氧化成醛的有
,根据已知信息,试回答分子式是C4H10O的醇可被氧化成醛的有