700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)?CO2(g)+H2(g)反应过程中测定的部分数据见下表(表中t2>t1):
下列说法正确的是( )
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
A、反应在t1 min内的平均速率为v(H2)=
| ||
| B、保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2O,达到平衡时n(CO2)=0.30 mol | ||
| C、保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大 | ||
| D、温度升高至800℃,上述反应平衡常数为0.64,则正反应为吸热反应 |
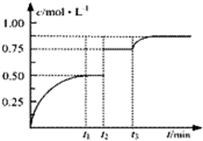 一定温度下,将1molA和1molB气体充入2L密闭容器,发生反应:A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确是( )
一定温度下,将1molA和1molB气体充入2L密闭容器,发生反应:A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确是( )| A、t1~t3间该反应的平衡常数均为4 |
| B、反应方程式中的x=1 |
| C、t2时刻改变的条件是使用催化剂 |
| D、t3时刻改变的条件是移去少量物质D |
金属镍有广泛的用途.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述不正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)( )
| A、阳极发生还原反应,其电极反应式为:Ni2++2e-═Ni |
| B、电解过程中,阳极质量的减少与阴极质量的增加不相等,但阴阳两极得失电子数目相等 |
| C、电解后,溶液中存在的金属阳离子有Ni2+、Fe2+和Zn2+ |
| D、电解后,电解槽底部的阳极泥中有Cu和Pt |
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,下列选项错误的( )
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,下列选项错误的( )| A、Y电极上的电极反应式为2Cl--2e-=Cl2↑.检验该电极反应产物的方法是把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色 | ||||
B、电解池中X极上的电极反应式为2H2O
| ||||
| C、如要用电解方法精炼粗铜,电解液a换用CuSO4溶液,则X电极的材料是精铜 | ||||
| D、若想用电解实验制得白色纯净的Fe(OH)2沉淀,a仍是饱和NaCl溶液,往U形管添加完饱和NaCl溶液后需加入少量苯,苯的作用是防止生成的Fe(OH)2被空气氧化 |
哥本哈根世界气候大会上,商讨了《京都议定书》一期承诺到期后的后续方案,即2012年至2020年的全球减排协议.大会倡导“节能减排”和“低碳经济”.下列做法不符合这一理念的是( )
| A、推广利用CO2与环氧丙烷和琥珀酸酐的三元共聚物的生物降解材料 |
| B、使用填埋法处理未经分类的生活垃圾 |
| C、推广煤的干馏、气化、液化技术,提供清洁、高效燃料和基础化工原料 |
| D、发展水电,开发新能源,如核能、太阳能、风能等,减少对化石能源的依赖 |
下列有关用惰性电极电解AgNO3溶液的说法不正确的是( )
| A、电解过程中阴极质量不断增大 |
| B、电解过程中阳极附近的pH不断降低 |
| C、电解一段时间后,向溶液中加入适量的Ag2O固体可使溶液恢复到电解前的状况 |
| D、电解过程中,溶液中电子由阴极迁向阳极 |
将镁、铝、硅的混合物分为等质量的两份.一份与足量NaOH溶液反应,另一份与足量盐酸反应,最后生成的氢气一样多.则镁与硅物质的量之比为( )
| A、2:1 | B、4:1 |
| C、1:1 | D、3:1 |
人类只有一个地球,保护地球环境人人有责.下列做法能达到相应目的是( )
| A、及时焚烧废弃塑料减少“白色污染” |
| B、工厂用高烟囱排放废气防止“酸雨” |
| C、使用车用乙醇汽油防止“温室效应” |
| D、推广使用无氟冰箱防止“臭氧空洞” |
下列措施有利于节能减排、改善环境质量的有( )
①发展核电,以减少火力发电带来的二氧化硫和二氧化碳排放问题
②积极推行“限塑令”,加快研发利用二氧化碳合成的聚碳酸酯类可降解塑料
③加速建设地铁、轻轨等轨道交通,减少汽车尾气排放
④发展低碳经济、循环经济,推广可利用太阳能、风能的城市照明系统
⑤使用生物酶降解生活废水中的有机物,使用填埋法处理未经分类的生活垃圾.
①发展核电,以减少火力发电带来的二氧化硫和二氧化碳排放问题
②积极推行“限塑令”,加快研发利用二氧化碳合成的聚碳酸酯类可降解塑料
③加速建设地铁、轻轨等轨道交通,减少汽车尾气排放
④发展低碳经济、循环经济,推广可利用太阳能、风能的城市照明系统
⑤使用生物酶降解生活废水中的有机物,使用填埋法处理未经分类的生活垃圾.
| A、①②③④ | B、①②⑤ |
| C、①②④⑤ | D、③④⑤ |
