德国著名行业杂志《应用化学》上刊登文章介绍:某中德联合研究小组设计制造了一种“水瓶”,用富勒烯(C60)的球形笼子作“瓶体”,一种磷酸盐作“瓶盖”,恰好可将一个水分子关在里面.下列说法正确的是( )
| A、水、双氧水、水玻璃都是纯净物 |
| B、石墨和C60互称为同位素 |
| C、磷酸是强电解质 |
| D、一定条件下石墨转化为C60是化学变化 |
将下列物质按酸、碱、盐分类排列,正确的是( )
| A、硫酸、纯碱、食盐 |
| B、磷酸、熟石灰、苛性钠 |
| C、碳酸、乙醇、醋酸钠 |
| D、盐酸、烧碱、胆矾 |
下列各组物质,按化合物、单质、混合物顺序排列的是( )
| A、烧碱、液态氧、铁矿石 |
| B、生石灰、白磷、熟石灰 |
| C、干冰、铜、氯化氢 |
| D、空气、氮气、胆矾 |
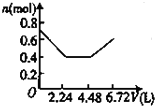
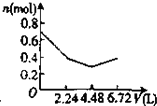
 将0.20mol NO和0.1mol CO充入一个容积恒定为1L的密闭容器中发生反应:
将0.20mol NO和0.1mol CO充入一个容积恒定为1L的密闭容器中发生反应:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0在不同条件下,反应过程中部分物质的浓度变化如图所示.下列说法正确的是( )
| A、容器内的压强不发生变化说明该反应达到平衡 |
| B、当向容器中再充入0.20 mol NO时,平衡向正反应方向移动,K增大 |
| C、第12 min时改变的反应条件为升高温度 |
| D、向该容器内充入He气,容器内气体压强增大,所以反应速率增大 |
不能实现下列物质间直接转化的元素是( )
单质氧化物
氧化物
酸或碱
盐.
单质氧化物
| +O2 |
| +H2O |
| +NaOH或HCl |
| A、氮 | B、硫 | C、碳 | D、铁 |
将下列各组物质按酸、碱、盐的顺序排列正确的是( )
| A、硫酸、纯碱、石膏 |
| B、氢硫酸、烧碱、绿矾 |
| C、硫酸、乙醇、醋酸钠 |
| D、磷酸、熟石灰、苛性钾 |
下列关于胶体的说法中正确的是( )
| A、胶体外观不均匀 |
| B、胶体不能通过滤纸 |
| C、胶体粒子不停地无秩序运动 |
| D、胶体不稳定,静止后容易形成沉淀 |
下列说法中正确的是(NA表示阿伏加德罗常数)( )
| A、4℃时,5.4mL水中所含的水分子数是0.3NA(4℃时,水的密度为1.0g/ml) |
| B、在常温常压下,11.2L氯气所含的原子数为NA |
| C、标准状况下,22.4L氢气所含的质子数为2 NA |
| D、2L 1mol?L-1K2SO4溶液中离子的总数为3 NA |