题目内容
下列说法中正确的是(NA表示阿伏加德罗常数)( )
| A、4℃时,5.4mL水中所含的水分子数是0.3NA(4℃时,水的密度为1.0g/ml) |
| B、在常温常压下,11.2L氯气所含的原子数为NA |
| C、标准状况下,22.4L氢气所含的质子数为2 NA |
| D、2L 1mol?L-1K2SO4溶液中离子的总数为3 NA |
考点:阿伏加德罗常数
专题:
分析:A、依据n=
计算物质的量得到分子数;
B、依据气体摩尔体积的条件分析判断,标准状况气体摩尔体积为22.4L/mol;
C、标准状况气体摩尔体积为22.4L/mol,n=
,结合分子式计算质子数;
D、硫酸钾完全电离,溶质物质的量n=CV,结合电离计算溶液中离子数.
| m |
| M |
B、依据气体摩尔体积的条件分析判断,标准状况气体摩尔体积为22.4L/mol;
C、标准状况气体摩尔体积为22.4L/mol,n=
| V |
| 22.4 |
D、硫酸钾完全电离,溶质物质的量n=CV,结合电离计算溶液中离子数.
解答:
解:A、4℃时,5.4mL水质量为5.4g,依据n=
计算物质的量=
=0.3mol,得到分子数0.3NA,故A正确;
B、依据气体摩尔体积的条件分析判断,标准状况气体摩尔体积为22.4L/mol,在常温常压下,11.2L氯气物质的量不是0.5mol,故B错误;
C、标准状况气体摩尔体积为22.4L/mol,n=
=
=1mol,结合分子式计算质子数为2 NA,故C正确;
D、硫酸钾完全电离,溶质物质的量n=CV=2L×1mol?L-1 =2mol,结合电离计算溶液中离子数4molK+,2molSO42-,水电离出氢离子和氢氧根离子,溶液中离子的总数大于6 NA,故D错误;
故选AC.
| m |
| M |
| 5.4g |
| 18g/mol |
B、依据气体摩尔体积的条件分析判断,标准状况气体摩尔体积为22.4L/mol,在常温常压下,11.2L氯气物质的量不是0.5mol,故B错误;
C、标准状况气体摩尔体积为22.4L/mol,n=
| V |
| 22.4 |
| 22.4L |
| 22.4L/mol |
D、硫酸钾完全电离,溶质物质的量n=CV=2L×1mol?L-1 =2mol,结合电离计算溶液中离子数4molK+,2molSO42-,水电离出氢离子和氢氧根离子,溶液中离子的总数大于6 NA,故D错误;
故选AC.
点评:本题考查了阿伏伽德罗常数的分析判断,主要是气体摩尔体积的条件分析应用,注意物质的量和各量的计算分析,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
下列微粒中,只有氧化性的是( )
①S2- ②Fe2+ ③Fe3+ ④S ⑤H+ ⑥Na+ ⑦Mg.
①S2- ②Fe2+ ③Fe3+ ④S ⑤H+ ⑥Na+ ⑦Mg.
| A、①⑦ | B、②④ |
| C、③⑤⑥ | D、②④⑤⑥ |
下列离子方程式书写正确的是( )
| A、用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-=Mn2++Cl2↑+2H2O |
| B、硫酸溶液与氢氧化钡溶液混合:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| C、Cu溶于足量浓硝酸:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O |
| D、FeCl3溶液与Cu反应:Fe3++Cu=Fe2++Cu2+ |
下列离子方程式书写正确的是( )
| A、Cu与AgNO3溶液反应:Cu+2Ag+=Cu2++2Ag |
| B、CaCO3和盐酸反应:CO32-+2H+=H2O+CO2↑ |
| C、Fe和稀H2SO4反应:2Fe+6H+=2Fe3++3H2↑ |
| D、Ba(OH)2与稀H2SO4反应:OH-+H++Ba2++SO42-=BaSO4↓+H2O |
下列说法错误的是( )
A、用数轴表示分散系的分类: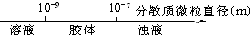 |
| B、已知氯酸钾与蔗糖(C12H22O11)反应的产物为KCl、CO2和水,则氧化产物与还原产物的物质的量之比为2:3 |
| C、10mL质量分数为98%的H2SO4,用10mL水稀释后,H2SO4的质量分数大于49% |
| D、可以用Ba(OH)2和焰色反应鉴别NaHCO3、NaCl、KCl、K2SO4 |
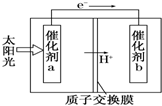 人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )| A、催化剂b表面的反应是CO2+2H++2e-═HCOOH |
| B、催化剂a表面发生氧化反应,有O2产生 |
| C、催化剂a附近酸性减弱,催化剂b附近酸性增强 |
| D、该过程是将太阳能转化为化学能的过程 |