题目内容
 将0.20mol NO和0.1mol CO充入一个容积恒定为1L的密闭容器中发生反应:
将0.20mol NO和0.1mol CO充入一个容积恒定为1L的密闭容器中发生反应:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0在不同条件下,反应过程中部分物质的浓度变化如图所示.下列说法正确的是( )
| A、容器内的压强不发生变化说明该反应达到平衡 |
| B、当向容器中再充入0.20 mol NO时,平衡向正反应方向移动,K增大 |
| C、第12 min时改变的反应条件为升高温度 |
| D、向该容器内充入He气,容器内气体压强增大,所以反应速率增大 |
考点:化学反应速率变化曲线及其应用,化学平衡的影响因素
专题:化学平衡专题
分析:A、反应前后气体体积减小,当容器内的压强不发生变化,说明该反应达到平衡;
B、当向容器中加再充入0.20mol NO时,平衡向正反应方向移动,K值不变;
C、正反应为放热反应,升高温度平衡向逆反应方向移动,氮气浓度减小,NO、CO浓度增大;
D、向该容器内充入He气,总压增大,气体分压不变,所以反应反应速率不变.
B、当向容器中加再充入0.20mol NO时,平衡向正反应方向移动,K值不变;
C、正反应为放热反应,升高温度平衡向逆反应方向移动,氮气浓度减小,NO、CO浓度增大;
D、向该容器内充入He气,总压增大,气体分压不变,所以反应反应速率不变.
解答:
解:A、反应前后气体体积减小,当容器内的压强不发生变化,说明该反应达到平衡,故A正确;
B、当向容器中加再充入0.20mol NO时,平衡向正反应方向移动,K值不变,故B错误;
C、正反应为放热反应,升高温度平衡向逆反应方向移动,氮气浓度减小,NO、CO浓度增大,和图象符合,故C正确;
D、向该容器内充入He气,总压增大,气体分压不变,所以反应反应速率不变,故D错误.
故选:AC.
B、当向容器中加再充入0.20mol NO时,平衡向正反应方向移动,K值不变,故B错误;
C、正反应为放热反应,升高温度平衡向逆反应方向移动,氮气浓度减小,NO、CO浓度增大,和图象符合,故C正确;
D、向该容器内充入He气,总压增大,气体分压不变,所以反应反应速率不变,故D错误.
故选:AC.
点评:本题考查了化学平衡状态的判断,化学反应速率的影响因素,难度不大,注意相关基础知识的积累.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
下列说法中正确的是( )
| A、丙烯分子中有8个σ键,1个π键 |
| B、在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 |
| C、NF3的沸点比NH3的沸点低得多,是因为NH3分子间有氢键,NF3只有范德华力 |
| D、NCl3和BC13分子中,中心原子都采用sp3杂化 |
下列离子方程式正确的是( )
| A、氢氧化镁中滴加盐酸:H++OH-═H2O |
| B、在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| C、已知电离平衡常数:H2CO3>HClO>HCO3-,向次氯酸钠溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO32- |
| D、向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液,恰好使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-═Al(OH)3↓+NH3?H2O+2BaSO4↓ |
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、2molNa被完全氧化生成1mol Na2O2,得到2NA个电子 |
| B、在1L0.1mol/L的碳酸钠溶液中,阴离子总数大于0.1NA |
| C、标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
| D、在KIO3+6HI=KI+3I2+3H2O反应中,每生成3mol I2,则转移6NA个电子 |
下列关于胶体的说法中正确的是( )
| A、胶体外观不均匀 |
| B、胶体不能通过滤纸 |
| C、胶体粒子不停地无秩序运动 |
| D、胶体不稳定,静止后容易形成沉淀 |
将两支惰性电极插入CuSO4溶液中,通电电解,当有1×10-3mol的OH-放电时,溶液显浅蓝色,则下列叙述正确的是( )
| A、阳极上析出5.6mL O2(标准状况) |
| B、阴极上析出64mg Cu |
| C、阴极上析出11.2mL H2(标准状况) |
| D、阳极和阴极质量都无变化 |
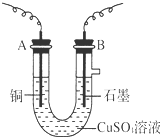 某化学兴趣小组用电解CuSO4溶液的方法,测定铜的相对原子质量.(装置如图所示)
某化学兴趣小组用电解CuSO4溶液的方法,测定铜的相对原子质量.(装置如图所示)