利用如图装置,完成很多电化学实验.下列有关此装置的叙述中,不正确的是( )


| A、若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法 |
| B、若X为碳棒,Y为饱和NaOH溶液,开关K置于N处,保持温度不变,则溶液的pH保持不变 |
| C、若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动 |
| D、若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小 |
一定温度下,向aL的密闭容器中加入2mol NO2(g),发生如下反应:2NO2?2NO+O2,此反应达到平衡的标志是( )
| A、单位时间内生成2n mol NO同时生成2n mol NO2 |
| B、混合气体中NO2、NO和O2的物质的量之比为2﹕2﹕1 |
| C、单位时间内生成2n mol NO同时生成n mol O2 |
| D、混合气体的颜色变浅 |
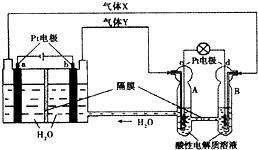 空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )| A、当有0.2mol电子转移时,a极产生1.12L O2 |
| B、该装置开始工作后,右端装置能量变化为:电能→化学能 |
| C、d极上发生的电极反应是:O2+4H++4e一═2H2O |
| D、c极上进行还原反应,B中的H+可以通过隔膜进入A |
含有砒霜(As2O3)的试样和锌、盐酸混合反应,生成的砷化氢(AsH3)在热玻璃管中完全分解成单质砷和氢气.若砷的质量为1.50g,则( )
| A、被氧化的砒霜为1.98 g |
| B、分解产生的氢气为672 mL |
| C、和砒霜反应的锌为3.90 g |
| D、转移的电子总数为0.06NA |
在pH=12的溶液中能大量共存且溶液为无色透明的离子组是( )
| A、K+、MnO4-、Na+、Cl- |
| B、SO42-、Na+、NO3-、CO32- |
| C、Na+、HCO3-、NO3-、SO42- |
| D、Fe3+、Na+、Cl-、SO42- |
某无色溶液中滴入酚酞试液显红色,该溶液中可以大量共存的离子组是( )
| A、Mg2+、Al3+、HCO3-、SO32- |
| B、K+、Ca2+、MnO4-、Cl- |
| C、Ba2+、Na+、AlO2-、NO3- |
| D、NH4+、Fe3+、SO42-、SCN- |
在CH3COOH?CH3COO-+H+的电离平衡中,要使电离平衡右移,且pH减小,应采取的措施( )
| A、增加NaOH | B、加热 |
| C、加水 | D、加浓盐酸 |
 某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)FeO(s)+CO(g)△H=a kJ?mol-1,测得CO2和CO浓度随时间的变化如图所示:
某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)FeO(s)+CO(g)△H=a kJ?mol-1,测得CO2和CO浓度随时间的变化如图所示: