将铜片投入到稀硫酸中,铜片不溶,加入下列试剂后,可使铜片溶解的是( )
| A、稀盐酸 | B、硫酸钠晶体 |
| C、硝酸钠晶体 | D、氯化铁晶体 |
在稀硫酸中加入铜粉,铜粉不溶解,再加入某X物质,发现铜粉逐渐溶解,问神秘的X不可能是( )
| A、FeCl3 |
| B、HNO3 |
| C、HCl |
| D、KNO3 |
铜粉放入稀硫酸溶液中,加热后无明显现象发生.当加入或通入下列某物质后,铜粉的质量保持不变,则该物质是( )
| A、Fe2 (SO4)3 |
| B、O2 |
| C、Cu (NO3)2 |
| D、FeCl2 |
下列叙述正确的是( )
| A、6.4gCu与足量硫完全反应,转移的电子数为0.1NA |
| B、能使湿润的KI淀粉试纸变蓝的气体一定是Cl2 |
| C、分离Na2CO3溶液和CH3COOC2H5常用蒸馏法 |
| D、将H2S通入FeCl3溶液中会产生淡黄色沉淀,继续通入则会产生黑色沉淀 |
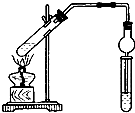 用如图所示实验装置制取乙酸乙酯.回答以下问题:
用如图所示实验装置制取乙酸乙酯.回答以下问题: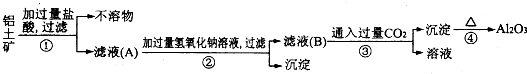
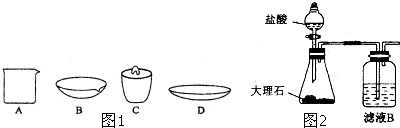
 如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置.
如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置.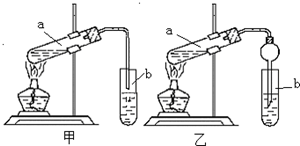 某实验小组欲制取乙酸乙酯,设计了如下图所示的装置,请回答有关问题:
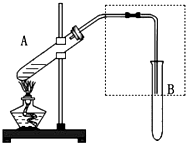
某实验小组欲制取乙酸乙酯,设计了如下图所示的装置,请回答有关问题: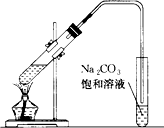 如图是实验室制乙酸乙酯的装置.
如图是实验室制乙酸乙酯的装置.