下列电离方程式中,书写错误的是( )
| A、Na2CO3=Na++CO32- |
| B、Ba(OH)2=Ba2++2OH- |
| C、H2SO4=2H++SO42- |
| D、KCl=K++Cl- |
下列电离方程式书写错误的是( )
| A、H2SO4=2H++SO42- |
| B、Al2(SO4)3=2Al3++3 SO42- |
| C、NaHCO3=Na++H++CO32- |
| D、Ba(OH)2=Ba2++2 OH- |
设NA代表阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下11.2LO2和16gO3中含有的氧原子数均为 NA |
| B、2.4g金属镁变成镁离子(Mg2+)时失去的电子数目的0.1NA |
| C、2g氢气所含原子数目为NA |
| D、1mol/L的CaCl2溶液中含有的Cl-为2NA |
已知下列氧化剂均能氧化+4价的硫(元素),为了除去稀硫酸中的亚硫酸,宜选用的氧化剂是( )
| A、氯气 | B、双氧水 |
| C、过氧化钠 | D、高锰酸钾 |
下列物质溶于水的电离方程式正确的是( )
| A、KHCO3═K++H++CO32- |
| B、H2S═2H++S2- |
| C、KHSO4═K++H++SO42- |
| D、Ba(OH)2=Ba2++(OH)2- |
下列叙述中能肯定说明金属A比金属B的活泼的是( )
| A、A原子最外层电子数比B原子的最外层电子数少 |
| B、A原子电子层数比B原子的电子层数多 |
| C、1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多 |
| D、常温时,A能从酸中置换出氢,而B不能 |
设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A、常温常压下,总质量为48 g 的氧气和臭氧混合气体中所含氧原子总数为3 NA |
| B、标准状况下,11.2 L SO3中所含分子数为0.5NA |
| C、1 mol SiO2中含有的Si-O单键数为2NA |
| D、8.7gMnO2与50mL 8mol/L浓盐酸充分反应后,生成Cl2的氯分子数为0.1NA |
向等量的NaOH溶液中分别通入CO2气体.因CO2的通入量不同,得到组分不同的溶液M.若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)关系如下,(注:①假设CO2全部逸出;②C图中oa=ab).其中M中只有1种溶质的是( )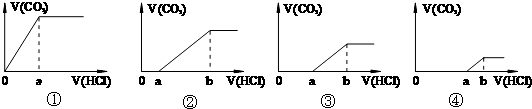

| A、只有① | B、只有③ |
| C、②④ | D、①③ |
设NA为阿伏伽德罗常数的数值,下列说法错误的是( )
| A、1molFe2+与足量的H2O2溶液反应,转移2NA个电子 |
| B、46gNO2和N2O4混合气体中含有原子总数为3NA |
| C、1 mol Na 与足量O2 反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
| D、1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023 |