题目内容
下列叙述中能肯定说明金属A比金属B的活泼的是( )
| A、A原子最外层电子数比B原子的最外层电子数少 |
| B、A原子电子层数比B原子的电子层数多 |
| C、1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多 |
| D、常温时,A能从酸中置换出氢,而B不能 |
考点:常见金属的活动性顺序及其应用
专题:
分析:金属活动性强弱的判断方法有:金属之间的置换反应、金属和酸或水反应置换出氢气的难易程度、金属的最高价氧化物的水化物碱性强弱等,据此分析解答.
解答:
解:A.A原子最外层电子数比B原子的最外层电子数少不能说明A的金属性大于B,如Ca的活泼性大于Li,故A错误;
B.A原子电子层数比B原子的电子层数多不能说明A的金属性大于B,如Cu不如Mg活泼,故B错误;
C.1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多不能说明A的金属性大于B,如Al不如Mg活泼,故C错误;
D.常温时,A能从酸中置换出氢,而B不能,说明A易失电子、B不易失电子,所以A的活泼性大于B,故D正确;
故选D.
B.A原子电子层数比B原子的电子层数多不能说明A的金属性大于B,如Cu不如Mg活泼,故B错误;
C.1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多不能说明A的金属性大于B,如Al不如Mg活泼,故C错误;
D.常温时,A能从酸中置换出氢,而B不能,说明A易失电子、B不易失电子,所以A的活泼性大于B,故D正确;
故选D.
点评:本题考查金属活泼性强弱判断,知道金属活泼性强弱判断的方法,注意:不能根据金属失电子多少判断金属性强弱,要根据金属失电子难易程度判断金属性强弱,为易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法正确的是( )
| A、原子晶体中只存在非极性共价键 |
| B、稀有气体形成的晶体属于分子晶体 |
| C、干冰升华时,分子内共价键会发生断裂 |
| D、分子晶体的熔点普遍都很高 |
下列有机物命名正确的是( )
A、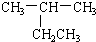 2-乙基丙烷 2-乙基丙烷 |
| B、CH3CH(CH3)CH3 2-甲基丙烷 |
C、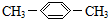 间二甲苯 间二甲苯 |
D、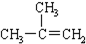 2-甲基-2-丙烯 2-甲基-2-丙烯 |
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、46g NO2和N2O4混合气体中含有原子总数为3 NA |
| B、1L0.1 mol/L的氨水含有0.1 NA个OH- |
| C、标准状况下,2.24L水含有分子的数目为0.1 NA |
| D、18gNH4+中所含的电子数为11 NA |
NA表示阿佛加德罗常数,下列说法正确的是( )
| A、1mol 任何气体的体积都约是22.4L |
| B、18gNH4+含有电子数为11NA |
| C、NA个H2SO4分子的质量与H3PO4的摩尔质量在数值上相等 |
| D、标准状况下,相同体积的O2、HCl、H2O含有的分子数相同 |
下列电离方程式中,书写错误的是( )
| A、Na2CO3=Na++CO32- |
| B、Ba(OH)2=Ba2++2OH- |
| C、H2SO4=2H++SO42- |
| D、KCl=K++Cl- |
下列离子方程式中,正确的是( )
| A、Cu(OH)2与稀盐酸反应:Cu(OH)2+2H+=Cu2++2H2O |
| B、氧化钠与水反应:Na2O+2H2O=Na++2OH- |
| C、铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| D、大理石溶于醋酸的反应:CaCO3+H+=Ca2++CO2↑+H2O |
下列变化必须加入其他物质作还原剂才能发生的是( )
| A、CuO→CuCl2 |
| B、H2O→H2 |
| C、I-→I2 |
| D、CO2→CO |
实验室可利用硫酸厂炉渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4?7H2O),聚铁的化学式为[Fe2(OH)n(SO4)3-0.5n]m,制备过程如图所示:下列说法不正确的是( )
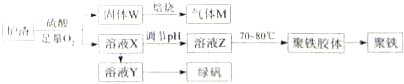

| A、炉渣中FeS与硫酸和氧气的反应式为:4FeS+3O2+12H+═4Fe3++4S↓+6H2O |
| B、气体M的成分是SO2,通入双氧水得到硫酸,可循环使用 |
| C、溶液Z的pH影响聚铁中铁的质量分数,若其pH偏小,将导致聚铁中铁的质量分数偏大 |
| D、向溶液X中加入过量铁粉,充分反应后过滤得到溶液Y,再经蒸发浓缩、冷却结晶、过滤等步骤得到绿矾 |